Πώς θα φτιάξατε 100cm3 από 0 01 mol dm3 θειικό χαλκό από ένα διάλυμα 1 θειικό;
Κατανόηση των εννοιών
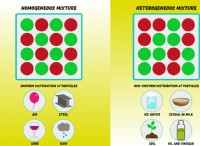
* Μοριακή (mol/dm3): Αυτό αντιπροσωπεύει τη συγκέντρωση ενός διαλύματος, που μας λέει τον αριθμό των γραμμομορίων διαλυμένης ουσίας που διαλύονται σε ένα κυβικό δεκαδμετρο (dm³) διαλύματος.
* αραίωση: Η διαδικασία μείωσης της συγκέντρωσης ενός διαλύματος προσθέτοντας περισσότερο διαλύτη (συνήθως νερό).
Υπολογισμοί
1. Προσδιορίστε τον όγκο του απαιτούμενου διαλύματος αποθέματος:
* Θέλετε τελικό όγκο 100 cm3 (0,1 dm3) σε συγκέντρωση 0,01 mol/dm3.
* Χρησιμοποιήστε τον τύπο:m₁v₁ =m₂v₂
* M₁ =συγκέντρωση του διαλύματος αποθέματος (1 mol/dm3)
* V₁ =όγκος του απαιτούμενου διαλύματος αποθέματος (άγνωστο)
* M₂ =συγκέντρωση του τελικού διαλύματος (0,01 mol/dm3)
* V₂ =τελικός όγκος του διαλύματος (0,1 dm3)
* Αντικαταστήστε τις τιμές:(1 mol/dm³) * v₁ =(0,01 mol/dm³) * (0,1 dm3)
* Λύστε για V₁:V₁ =0.001 dm3 ή 1 cm³
2. Προετοιμάστε το αραιωμένο διάλυμα:
* Μετρήστε 1 cm3 του διαλύματος θειικού χαλκού 1 mol/dm3 χρησιμοποιώντας έναν διαβαθμισμένο κύλινδρο ή πιπέτα.
* Προσθέστε αυτό το 1 cm³ αποθεμάτων σε μια ογκομετρική φιάλη.
* Προσθέστε προσεκτικά αποσταγμένο νερό στη φιάλη έως ότου ο συνολικός όγκος φτάσει τα 100 cm³.
* Σταματήστε τη φιάλη και ανακατέψτε καλά για να εξασφαλίσετε ένα ομοιογενές διάλυμα.
προφυλάξεις ασφαλείας
* Φορέστε κατάλληλα γυαλιά ασφαλείας και γάντια κατά τη διαχείριση των χημικών ουσιών.
* Εργαστείτε σε μια καλά αεριζόμενη περιοχή.
* Προσθέστε πάντα οξύ στο νερό, ποτέ δεν νερό σε οξύ.
Σημαντικές σημειώσεις
* Οι υπολογισμοί υποθέτουν ότι η πυκνότητα του αποθέματος είναι περίπου 1 g/cm3. Εάν έχετε διαφορετική πυκνότητα, ίσως χρειαστεί να ρυθμίσετε ελαφρώς τους όγκους.
* Βεβαιωθείτε ότι η ογκομετρική φιάλη σας είναι καθαρή και στεγνή πριν από τη χρήση.
* Το τελικό διάλυμα θα είναι 0,01 mol/dm3 θειικό χαλκό, το οποίο ισοδυναμεί με 10 mmol/dm3 ή 10 mm.