Διαφορά μεταξύ υπεροξειδίου και υπεροξειδίου του υδρογόνου
Κύρια διαφορά – Υπεροξείδιο έναντι υπεροξειδίου του υδρογόνου
Υπεροξείδιο είναι κάθε ένωση που αποτελείται από έναν απλό δεσμό οξυγόνου-οξυγόνου. Αυτό μπορεί να είναι είτε με τη μορφή ενός ανιόντος είτε μεταξύ άλλων ατόμων του μορίου. Το υπεροξείδιο του υδρογόνου είναι το απλούστερο υπεροξείδιο που μπορεί να βρεθεί. Αποτελείται από δύο άτομα υδρογόνου και δύο άτομα οξυγόνου. Αυτά τα δύο άτομα οξυγόνου συνδέονται μεταξύ τους μέσω ενός μόνο δεσμού. Όταν υπάρχουν διαφορετικά άτομα συνδεδεμένα με τον δεσμό οξυγόνου-οξυγόνου αντί για άτομα υδρογόνου, τότε ονομάζονται ανάλογα με τον τύπο των ατόμων ή τις ομάδες ατόμων που συνδέονται με αυτόν τον μοναδικό δεσμό. Ωστόσο, αυτά τα υπεροξείδια διαφέρουν μεταξύ τους στις χημικές και φυσικές τους ιδιότητες. Η κύρια διαφορά μεταξύ του υπεροξειδίου και του υπεροξειδίου του υδρογόνου είναι ότι τα υπεροξείδια μπορεί να είναι είτε ιοντικές ή ομοιοπολικές ενώσεις, ενώ το υπεροξείδιο του υδρογόνου είναι ομοιοπολική ένωση.
Βασικές περιοχές που καλύπτονται
1. Τι είναι το υπεροξείδιο
– Ορισμός, Ιδιότητες, Χρήσεις
2. Τι είναι το υπεροξείδιο του υδρογόνου
– Ορισμός, Ιδιότητες, Χρήσεις
3. Ποιες είναι οι ομοιότητες μεταξύ του υπεροξειδίου και του υπεροξειδίου του υδρογόνου
– Περίληψη κοινών χαρακτηριστικών
4. Ποια είναι η διαφορά μεταξύ υπεροξειδίου και υπεροξειδίου του υδρογόνου
– Σύγκριση βασικών διαφορών
Βασικοί όροι:Ομοιοπολικές ενώσεις, υπεροξείδιο του υδρογόνου, ιοντικές ενώσεις, οξυγόνο, υπεροξείδιο 
Τι είναι το υπεροξείδιο
Υπεροξείδιο είναι οποιαδήποτε ένωση που αποτελείται από έναν απλό δεσμό οξυγόνου-οξυγόνου. Επομένως, το κύριο χαρακτηριστικό για την αναγνώριση μιας ένωσης υπεροξειδίου είναι η παρουσία αυτού του ομοιοπολικού δεσμού Ο-Ο. Μερικές φορές, αυτός ο δεσμός μπορεί να παρατηρηθεί ως ανιόν σε μια ιοντική ένωση. Στη συνέχεια δίνεται σε σύμβολα ως O2 . Αυτό ονομάζεται ανιόν υπεροξειδίου. Όταν ο δεσμός Ο-Ο βρίσκεται σε μια ομοιοπολική ένωση, ονομάζεται υπεροξοομάδα ή ομάδα υπεροξειδίου.
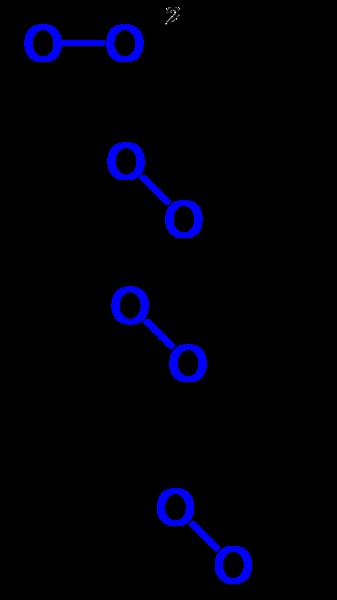
Εικόνα 1:Στα παραπάνω παραδείγματα, οι μπλε δεσμοί δείχνουν τις ομάδες υπεροξειδίου.
Στην ομάδα υπεροξειδίου, η κατάσταση οξείδωσης ενός ατόμου οξυγόνου είναι -1. Κανονικά το οξυγόνο προτιμά να δείχνει την κατάσταση οξείδωσης 0 ή -2. Αλλά επειδή υπάρχουν δύο άτομα οξυγόνου που συνδέονται μεταξύ τους, ένα άτομο οξυγόνου παίρνει κατάσταση οξείδωσης -1. Στο ανιόν υπεροξειδίου, ένα άτομο οξυγόνου έχει -1 ηλεκτρικό φορτίο αφού το συνολικό φορτίο του ανιόντος είναι -2.
Τα ιοντικά υπεροξείδια αποτελούνται από ένα ανιόν υπεροξειδίου συνδεδεμένο με ιόντα μετάλλων αλκαλίων ή ιόντα μετάλλου αλκαλικής γαίας ως κατιόν. Μερικά παραδείγματα είναι το υπεροξείδιο του νατρίου (Na2 O2 ), υπεροξείδιο του καλίου (K2 O2 ), υπεροξείδιο του μαγνησίου (MgO), κ.λπ. Οι ομοιοπολικές ενώσεις υπεροξειδίου αποτελούνται από απλό δεσμό Ο-Ο που συνδέεται άμεσα με άλλα άτομα του μορίου. για παράδειγμα, υπεροξείδιο του υδρογόνου (H2 O2 ) και υπεροξυμονοθειικό οξύ (H2 SO5 ).
Τα υπεροξείδια μπορούν να βρεθούν σε βιολογικά συστήματα και στη φύση. Για παράδειγμα, ορισμένα ένζυμα στα κύτταρά μας χρησιμοποιούν υπεροξείδια για να καταλύσουν ορισμένες αντιδράσεις. Ορισμένα είδη φυτών χρησιμοποιούν ενώσεις υπεροξειδίου ως χημικές ουσίες σηματοδότησης. Τα υπεροξείδια χρησιμοποιούνται επίσης σε εφαρμογές εργαστηριακής κλίμακας. Είναι πολύ χρήσιμο στην οργανική χημεία προκειμένου να ληφθεί το προϊόν anti-Markovnikov από μια οργανική αντίδραση.
Τι είναι το υπεροξείδιο του υδρογόνου
Το υπεροξείδιο του υδρογόνου είναι μια ομοιοπολική ένωση υπεροξειδίου με μοριακό τύπο H2 O2 . Είναι μια ομοιοπολική ένωση επειδή όλοι οι δεσμοί μεταξύ των τεσσάρων ατόμων είναι ομοιοπολικοί δεσμοί. Τα δύο άτομα οξυγόνου συνδέονται μεταξύ τους. Τα δύο άτομα υδρογόνου συνδέονται με τα άτομα οξυγόνου, ένα άτομο υδρογόνου ανά άτομο οξυγόνου. Η μοριακή μάζα του υπεροξειδίου του υδρογόνου είναι περίπου 34,014 g/mol.
Το υπεροξείδιο του υδρογόνου είναι ένα απαλό μπλε υγρό που έχει ελαφρώς διαφορετικό ιξώδες από το νερό. Θεωρείται ως ασθενές οξύ. Δεδομένου ότι έχει ισχυρές οξειδωτικές ιδιότητες, το υπεροξείδιο του υδρογόνου χρησιμοποιείται ως οξειδωτικός παράγοντας σε λευκαντικές ενώσεις. Το υπεροξείδιο του υδρογόνου είναι ασταθές. Αποσυντίθεται γρήγορα σε αέριο οξυγόνο και νερό.
Αν και η διαφορά μεταξύ ενός μορίου νερού και ενός μορίου υπεροξειδίου του υδρογόνου είναι απλώς ένα επιπλέον άτομο οξυγόνου που υπάρχει στον μοριακό τύπο του υπεροξειδίου του υδρογόνου, οι μοριακές δομές είναι πολύ διαφορετικές μεταξύ τους.
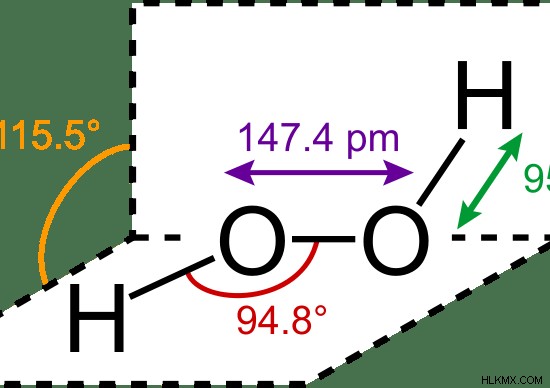
Εικόνα 2:Χημικές ιδιότητες του υπεροξειδίου του υδρογόνου
Το υπεροξείδιο του υδρογόνου χρησιμοποιείται σε βιομηχανικές εφαρμογές καθώς και σε ιατρικές εφαρμογές. Στη βιομηχανία, το υπεροξείδιο του υδρογόνου χρησιμοποιείται ως συστατικό λεύκανσης για λευκαντικούς παράγοντες. Σε ιατρικές εφαρμογές, χρησιμοποιείται ως απολυμαντικό. Εκτός από αυτό, μπορεί να χρησιμοποιηθεί και ως προωθητικό.
Ομοιότητες μεταξύ υπεροξειδίου και υπεροξειδίου του υδρογόνου
- Και οι δύο ενώσεις αποτελούνται από μονό δεσμό οξυγόνου-οξυγόνου.
- Και τα δύο είναι καλά οξειδωτικά μέσα.
Διαφορά μεταξύ υπεροξειδίου και υπεροξειδίου του υδρογόνου
Ορισμός
Υπεροξείδιο: Το υπεροξείδιο είναι οποιαδήποτε ένωση που αποτελείται από έναν απλό δεσμό οξυγόνου-οξυγόνου.
Υπεροξείδιο του υδρογόνου: Το υπεροξείδιο του υδρογόνου είναι μια ομοιοπολική ένωση υπεροξειδίου που έχει τον μοριακό τύπο H2 O2 .
Φύση
Υπεροξείδιο: Τα υπεροξείδια μπορεί να είναι είτε ιοντικές ενώσεις είτε ομοιοπολικές ενώσεις.
Υπεροξείδιο του υδρογόνου: Το υπεροξείδιο του υδρογόνου είναι μια ομοιοπολική ένωση.
Μοριακή μάζα
Υπεροξείδιο: Η μοριακή μάζα των υπεροξειδίων εξαρτάται από τα άτομα ή την ομάδα ατόμων που συνδέονται με τον δεσμό O-O.
Υπεροξείδιο του υδρογόνου: Η μοριακή μάζα του υπεροξειδίου του υδρογόνου είναι περίπου 34,014 g/mol.
Παρουσία ατόμων υδρογόνου
Υπεροξείδιο: Τα υπεροξείδια μπορεί να αποτελούνται ή να μην αποτελούνται από άτομα υδρογόνου συνδεδεμένα απευθείας με τον απλό δεσμό O-O.
Υπεροξείδιο του υδρογόνου: Το υπεροξείδιο του υδρογόνου αποτελείται ουσιαστικά από δύο άτομα υδρογόνου που συνδέονται με τον απλό δεσμό O-O.
Συμπέρασμα
Τα υπεροξείδια είναι ενώσεις που αποτελούνται από μονοπολικούς δεσμούς οξυγόνου-οξυγόνου. Το υπεροξείδιο του υδρογόνου είναι επίσης ένας τύπος ένωσης υπεροξειδίου. Οι ενώσεις υπεροξειδίου μπορούν να χωριστούν κυρίως σε δύο ομάδες ως ιοντικές και ομοιοπολικές ενώσεις. Αλλά το υπεροξείδιο του υδρογόνου είναι μια ομοιοπολική ένωση. Αυτή είναι η κύρια διαφορά μεταξύ του υπεροξειδίου και του υπεροξειδίου του υδρογόνου.