Τι θα ψάχνετε για να μάθετε αν μια ένωση είναι ιοντική ή ομοιοπολική;
Understanding the Basics
* Ιωνικές ενώσεις: Σχηματίζεται από την ηλεκτροστατική έλξη μεταξύ θετικά φορτισμένων ιόντων (κατιόντων) και αρνητικά φορτισμένων ιόντων (ανιόντες). Συνήθως περιλαμβάνουν ένα μέταλλο και ένα μέταλλο.
* ομοιοπολικές ενώσεις: Που σχηματίζονται από την κοινή χρήση ηλεκτρονίων μεταξύ δύο μη μεταλλικών.
δείκτες κλειδιού
1. Τύπος στοιχείων:
* Metal and Nonetal: Ένας ισχυρός δείκτης μιας ιοντικής ένωσης . Παραδείγματα:NaCl (χλωριούχο νάτριο), MGO (οξείδιο μαγνησίου).
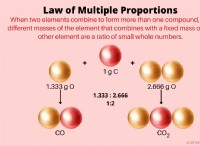
* Δύο μη μέταλλα: Ένας ισχυρός δείκτης μιας ομοιοπολικής ένωσης . Παραδείγματα:CO2 (διοξείδιο του άνθρακα), H2O (νερό).
2. Διαφορά ηλεκτροαρνητικότητας:
* Ηλεκτροργατιστικότητα: Ένα μέτρο της ικανότητας ενός ατόμου να προσελκύει ηλεκτρόνια σε έναν δεσμό.
* Μεγάλη διαφορά (ΔEN> 1,7): Τυπικά υποδεικνύει έναν ιονικό δεσμό (Ένα άτομο τραβά τα ηλεκτρόνια μακριά από το άλλο).
* Μικρή διαφορά (ΔEN <1,7): Συνήθως υποδεικνύει ένα ομοιοπολικό δεσμό (Τα ηλεκτρόνια μοιράζονται πιο εξίσου).
3. Φυσικές ιδιότητες:
* Ιωνικές ενώσεις:
* Συνήθως υψηλά σημεία τήξης και βρασμού.
* Συχνά κρυσταλλικά στερεά σε θερμοκρασία δωματίου.
* Διεξαγωγή ηλεκτρικής ενέργειας όταν διαλύεται σε νερό ή λιωμένο.
* ομοιοπολικές ενώσεις:
* Γενικά χαμηλότερα σημεία τήξης και βρασμού.
* Μπορεί να είναι στερεά, υγρά ή αέρια σε θερμοκρασία δωματίου.
* Κακοί αγωγοί ηλεκτρικής ενέργειας.
Πρόσθετες εκτιμήσεις
* Πολυατομικά ιόντα: Οι ενώσεις που περιέχουν ομάδες ατόμων με συνολικό φορτίο μπορεί να είναι ιοντικές (π.χ. Na2Co3, ανθρακικό νάτριο).
* Μεταλλική σύνδεση: Εμφανίζεται μεταξύ των ατόμων μετάλλων και είναι ξεχωριστό από ιοντική ή ομοιοπολική συγκόλληση.
Παράδειγμα
Ας αναλύσουμε την ένωση NaCl (χλωριούχο νάτριο):
* νάτριο (NA): Ένα μέταλλο.
* χλώριο (CL): Ένα μέταλλο.
* Μεγάλη διαφορά ηλεκτροαρνητικότητας: Το χλώριο έχει υψηλότερη ηλεκτροαρνητικότητα από το νάτριο.
* Φυσικές ιδιότητες: Το NaCl είναι ένα κρυσταλλικό στερεό υψηλής περιόδου, το οποίο διεξάγει ηλεκτρική ενέργεια όταν διαλύεται.
Συμπέρασμα: Με βάση αυτά τα χαρακτηριστικά, μπορούμε να ταξινομήσουμε με βεβαιότητα το NaCl ως ιοντική ένωση.
Ενημερώστε με αν έχετε συγκεκριμένες ενώσεις που θέλετε να αναλύσετε!