Πυκνότητα πιθανότητας
Σύμφωνα με την αρχή της αβεβαιότητας του Heisenberg, δεν μπορούμε ποτέ να γνωρίζουμε την ακριβή θέση ενός ηλεκτρόνιο που ταξιδεύει γύρω από τον πυρήνα με συγκεκριμένη ταχύτητα. Ως αποτέλεσμα, μιλάμε για την πιθανότητα εμφάνισής του σε οποιαδήποτε δεδομένη περιοχή. Με άλλα λόγια, χρησιμοποιούμε μια συνάρτηση πιθανότητας για να προσδιορίσουμε τη θέση της.
Γράφημα κατανομής πιθανότητας
Σχεδιάζοντας μια ενιαία κατανομή πιθανοτήτων
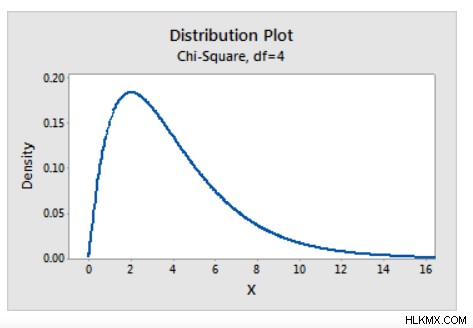
Σχεδιάζοντας μια κατανομή πιθανότητας με διαφορετικές παραμέτρους

Γράφημα κατανομής πιθανότητας δύο κατανομών
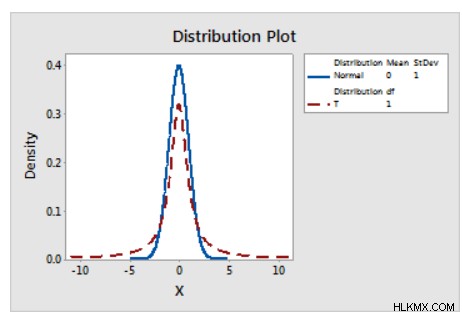
Συνάρτηση πυκνότητας πιθανότητας
Μπορείτε να υπολογίσετε την πιθανότητα ενός περιστατικού χρησιμοποιώντας τη συνάρτηση πυκνότητας πιθανότητας (PDF ) μιας τυχαίας μεταβλητής, X, ως εξής:
Η πιθανότητα ότι το X έχει τιμές στο διάστημα (a,b) για συνεχείς κατανομές ισούται με την περιοχή κάτω από το PDF του στο διάστημα (a,b).
Η πιθανότητα ότι το X έχει τιμές στο διάστημα (a,b) για οι διακριτές κατανομές είναι ίσες με το άθροισμα του PDF (γνωστό και ως συνάρτηση μάζας πιθανότητας) των δυνητικών διακριτών τιμών του X στο διάστημα (a,b) (a,b).
Προσδιορίστε την τιμή της συνάρτησης πυκνότητας πιθανότητας σε μια γνωστή τιμή x της τυχαίας μεταβλητής X χρησιμοποιώντας PDF.
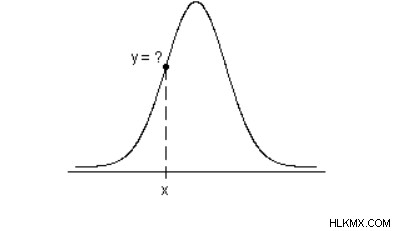
Τύπος κατανομής πιθανότητας
Οποιαδήποτε στατιστική συνάρτηση που καθορίζει όλα τα πιθανά αποτελέσματα μιας τυχαίας μεταβλητής μέσα σε ένα συγκεκριμένο Το εύρος τιμών αναφέρεται ως "κατανομή πιθανότητας". Η κανονική κατανομή είναι μια από τις πιο συχνές κατανομές πιθανοτήτων. Η κατανομή χ-τετράγωνο, η διωνυμική κατανομή και η κατανομή Poisson είναι τρεις ακόμη εξέχοντες τύποι κατανομών πιθανοτήτων.
Από την άλλη πλευρά, ο όρος "φόρμουλα κατανομής πιθανότητας" αναφέρεται στην τύπος για το μέσο όρο μιας κατανομής πιθανότητας, την τυπική απόκλιση, τη λοξότητα και την κύρτωση. Ο τύπος για τη μέση και τυπική απόκλιση, από την άλλη πλευρά, θα συζητηθεί σε αυτό το άρθρο.
Σε μια κατανομή πιθανότητας, ο μέσος όρος είναι η αναμενόμενη τιμή της τυχαίας μεταβλητής . Το άθροισμα των γινομένων της τιμής της τυχαίας μεταβλητής και της πιθανότητας της είναι ο τύπος για τον μέσο όρο μιας κατανομής πιθανότητας. Εκφράζεται μαθηματικά ως,
X = [ Xi * P(Xi)]
πού,
xi =Η τιμή της τυχαίας μεταβλητής στην ιη παρατήρηση
P(xi) υποδηλώνει την πιθανότητα της τιμής ith
Η τυπική απόκλιση είναι ένα μέτρο του πόσο μακριά αποκλίνει η τιμή κάθε τυχαίας μεταβλητής την αναμενόμενη αξία του. Η τετραγωνική ρίζα του αθροίσματος του γινομένου του τετραγώνου της απόκλισης κάθε τιμής από τη μέση τιμή και η πιθανότητα κάθε τιμής είναι ο τύπος για την τυπική απόκλιση. Εκφράζεται μαθηματικά ως,
=(Xi – X)2 * P(Xi)
Πυκνότητα πιθανότητας και σημασία του
Η θέση της περιοχής στο διάστημα όπου θέλουμε να βρούμε την πιθανότητα η ύπαρξη του ηλεκτρονίου θα αλλάξει τη συνάρτηση πιθανότητας. Η πιθανότητα να ανακαλυφθεί το ηλεκτρόνιο στο στοιχείο μικρού κυβικού όγκου της διάστασης dxdydz παρέχεται από το γινόμενο του 𑄺(x, y, z) και τον όγκο του στοιχείου μικρού κυβικού όγκου. δηλαδή από το 👄(x,y,z) dxdydz. Ένας κύβος με διαστάσεις de dy, de, με κέντρο το σημείο 👄(x, y, z) αντιπροσωπεύει το μικροσκοπικό στοιχείο όγκου. Γύρω από το σημείο sy, το στοιχείο μικρού όγκου ddyde γράφεται εναλλακτικά ως 1.
Η πυκνότητα πιθανότητας είναι ένα άλλο όνομα για τη συνάρτηση . Σκεφτείτε να διαιρέσετε ολόκληρο τον χώρο σε έναν αριθμό από αυτά τα κομμάτια όγκου. Το άθροισμα όλων των όρων της μορφής 👄dxdydz ή 👄d👁 θα δώσει ολόκληρη την πιθανότητα εντοπισμού του ηλεκτρονίου σε όλο το διάστημα. Ολόκληρη η πιθανότητα πρέπει να είναι ίση με τη μονάδα αφού το ηλεκτρόνιο πρέπει να βρίσκεται κάπου στο διάστημα. Έτσι,
– +d =– +dxdydz =1 (1)
Η ιδέα της πιθανότητας εξηγεί τον βασικό νόμο της φύσης ότι η επίγνωσή μας για ένα Η θέση του μικρού κινούμενου σωματιδίου δεν μπορεί ποτέ να είναι απόλυτη.
Ας υποθέσουμε ότι η λύση της κυματικής εξίσωσης για ένα μεμονωμένο σωματίδιο είναι μια συνάρτηση Ψ (x, y, z), η οποία αναφέρεται ως η κυματική συνάρτηση. Όπως αναφέρθηκε προηγουμένως, το εργοστάσιο συμβολίζει το πλάτος του κύματος. Από όσο μπορεί κανείς να πει, δεν έχει καμία φυσική σχέση. Είναι το τετράγωνο του πλάτους (Le significance μάλλον παρά το ίδιο το πλάτος (π.χ. Ψ) στην περίπτωση των κυμάτων).
Σκεφτείτε τη διπλή φύση της ηλεκτρομαγνητικής ακτινοβολίας. Σύμφωνα με την κυματική θεωρία, το τετράγωνο του πλάτους του κύματος, το οποίο μπορεί να υπολογιστεί λύνοντας την εφαρμοστέα κυματική εξίσωση, χρησιμοποιείται για τον υπολογισμό της έντασης της ακτινοβολίας. Η θεωρία φωτονίων συσχετίζει τον αριθμό των φωτονίων σε έναν ορισμένο όγκο, την πυκνότητα φωτονίων Le, με την ένταση της ακτινοβολίας. Επειδή τα φωτόνια είναι μικροσκοπικά σωματίδια, η πυκνότητά τους είναι ανάλογη με την πιθανότητα παρουσίας τους σε έναν δεδομένο όγκο, η οποία είναι γνωστή ως πυκνότητα πιθανότητας. Ως αποτέλεσμα, η πυκνότητα πιθανότητας, ή η πιθανότητα ανίχνευσης ενός φωτονίου σε έναν δεδομένο όγκο, είναι ανάλογη με το τετράγωνο του πλάτους του σχετικού κύματος. Κατ' αναλογία, λοιπόν, το Ψ (το τετράγωνο του πλάτους) θα είναι ένα μέτρο της πιθανότητας εύρεσης ηλεκτρονίου στον δεδομένο όγκο. Αντίστοιχα,
(x,y,z) ²( x. y. z) =k² (x, y, z) (2)
Θέτουμε την αναλογικότητα σταθερά &με τέτοιο τρόπο ώστε η ισότητα να αντικαθιστά την αναλογικότητα. Αν (x. y. z) είναι η λύση της κυματικής εξίσωσης Schrodinger για οποιοδήποτε σύστημα, τότε η ίδια λύση κυματικής εξίσωσης πολλαπλασιάζεται με οποιαδήποτε σταθερά. Ως αποτέλεσμα, μπορούμε να χρησιμοποιήσουμε (1k) αντί για την εξίσωση 2, με αποτέλεσμα:
👄(x,y,z) =k1k (x,y,z) =² (x. y. z) (3)
– +d =– +²d =1
( – +d =1 ) (4 )
Το Ο παράγοντας²d αντιπροσωπεύει την πιθανότητα εντοπισμού του ηλεκτρονίου στο στοιχείο μικρού όγκου d.
Το Electron Charge Cloud είναι μια ιδέα
Σκεφτείτε ένα άτομο υδρογόνου στη θεμελιώδη του κατάσταση , όπου ο πυρήνας του υδρογόνου και το μοναχικό του ηλεκτρόνιο είναι ορατά. Ας υποθέσουμε ότι ο πυρήνας παραμένει σε μια σταθερή θέση ενώ το ηλεκτρόνιο κινείται. Εάν ένα ηλεκτρόνιο μπορούσε να καταγράψει τη θέση του ως κουκκίδα κάθε 1/1000 του δευτερολέπτου για χίλια δευτερόλεπτα, η υψηλότερη συγκέντρωση τέτοιων κουκκίδων θα ήταν πιο κοντά στον πυρήνα και θα συνέχιζε να μειώνεται καθώς η απόσταση μεταξύ του πυρήνα και του ηλεκτρονίου μεγαλώνει σε όλες τις κατευθύνσεις.
Αυτό δείχνει ότι η καλύτερη πιθανότητα να βρεθούν τα ηλεκτρόνια είναι πιο κοντά στον πυρήνα και ότι η πιθανότητα εύρεσης τους μειώνεται όσο μεγαλώνει η απόσταση από τον πυρήνα. Πρέπει να σημειωθεί ότι η πραγματική θέση του ηλεκτρονίου δεν μπορεί να προσδιοριστεί. Το μόνο που μπορούμε να γνωρίζουμε είναι ένα συγκεκριμένο κομμάτι χώρου μέσα στο οποίο είναι δυνατή η παρουσία του ηλεκτρονίου. Το νέφος φορτίου ηλεκτρονίων αποτελείται από την κατανομή πιθανότητας ηλεκτρονίων σε τρισδιάστατο χώρο γύρω από τον πυρήνα. Η πιθανότητα εντοπισμού του ηλεκτρονίου είναι μεγαλύτερη στη θέση όπου ένα τέτοιο νέφος ηλεκτρονίων είναι πιο παχύ, δηλαδή όπου ο αριθμός των κουκκίδων που υποδεικνύουν τη θέση του ηλεκτρονίου είναι μεγαλύτερος.
Συμπέρασμα
Η συνάρτηση πυκνότητας πιθανότητας έχει επίσης αναφερθεί ως «συνάρτηση κατανομής πιθανότητας» και «συνάρτηση πιθανότητας». Ωστόσο, μεταξύ των πιθανοτήτων και των στατιστικολόγων, αυτή η χρήση δεν είναι κοινή. Σε άλλες πηγές, η "συνάρτηση κατανομής πιθανότητας" μπορεί να αναφέρεται στη συνάρτηση αθροιστικής κατανομής ή σε μια συνάρτηση μάζας πιθανότητας (PMF) αντί στην πυκνότητα όταν η κατανομή πιθανότητας περιγράφεται ως συνάρτηση σε γενικά σύνολα τιμών. Ο όρος «συνάρτηση πυκνότητας» εφαρμόζεται επίσης στη συνάρτηση μάζας πιθανότητας, προκαλώντας ακόμη μεγαλύτερη σύγχυση. Γενικά, το PMF χρησιμοποιείται με διακριτές τυχαίες μεταβλητές (τυχαίες μεταβλητές που λαμβάνουν τιμές από ένα μετρήσιμο σύνολο), ενώ το PDF χρησιμοποιείται με συνεχείς τυχαίες μεταβλητές. Μπορούμε μόνο οπτικά να κατανοήσουμε την κατανομή των δεδομένων εμφανίζοντας γραφήματα πυκνότητας πιθανότητας χωρίς να γνωρίζουμε την ακριβή πιθανότητα για ένα δεδομένο εύρος τιμών.




