Γιατί μερικά στερεά λιώνουν σε υψηλότερες θερμοκρασίες από άλλες;
* Διαμοριακές δυνάμεις: Αυτές οι δυνάμεις είναι τα αξιοθέατα μεταξύ των μορίων. Όσο ισχυρότερες είναι οι διαμοριακές δυνάμεις, τόσο περισσότερη ενέργεια απαιτείται για να τους σπάσει και να λιώσει το στερεό. Σκεφτείτε το σαν κόλλα που κρατάει τα πράγματα μαζί - η ισχυρότερη κόλλα χρειάζεται περισσότερη δύναμη για να σπάσει.
* δεσμός υδρογόνου: Ο ισχυρότερος τύπος διαμοριακής δύναμης, που περιλαμβάνει άτομα υδρογόνου που συνδέονται με εξαιρετικά ηλεκτροαρνητικά άτομα όπως οξυγόνο, άζωτο ή φθόριο.
* αλληλεπιδράσεις διπόλης-διπόλης: Αυτά συμβαίνουν μεταξύ πολικών μορίων, όπου υπάρχει ένας διαχωρισμός φορτίου.
* Δυνάμεις διασποράς του Λονδίνου: Αδύναμος τύπος, που υπάρχει σε όλα τα μόρια λόγω προσωρινών διακυμάνσεων στην κατανομή ηλεκτρονίων.
* Δομή κρυσταλλικού πλέγματος: Τη διάταξη μορίων ή ατόμων σε ένα στερεό. Μια πιο σφιχτά συσκευασμένη και διατεταγμένη δομή (όπως ένα κρυσταλλικό στερεό) θα έχει γενικά υψηλότερο σημείο τήξης από μια λιγότερο διατεταγμένη δομή (όπως ένα άμορφο στερεό).
* Μοριακό βάρος: Γενικά, τα βαρύτερα μόρια έχουν ισχυρότερες δυνάμεις διασποράς του Λονδίνου και υψηλότερα σημεία τήξης.
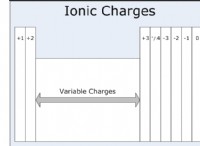
* Ιονικά ομόλογα: Στις ιοντικές ενώσεις, η ηλεκτροστατική έλξη μεταξύ των αντίθετα φορτισμένων ιόντων είναι πολύ ισχυρή. Αυτές οι ενώσεις έχουν συνήθως πολύ υψηλά σημεία τήξης.
* Μεταλλικοί δεσμοί: Τα μέταλλα έχουν μια θάλασσα ηλεκτρονίων, οδηγώντας σε ισχυρά αξιοθέατα και υψηλά σημεία τήξης.
Εδώ είναι μερικά παραδείγματα:
* νερό (H2O): Έχει ισχυρή δέσμευση υδρογόνου, δίνοντάς του ένα σχετικά υψηλό σημείο τήξης (0 ° C).
* Diamond (C): Ένα πολύ διατεταγμένο, ομοιοπολικό δίκτυο στερεά με ισχυρούς δεσμούς, δίνοντάς του ένα εξαιρετικά υψηλό σημείο τήξης (3550 ° C).
* Χλωριούχο νάτριο (NaCl): Μια ιοντική ένωση με ισχυρά ηλεκτροστατικά αξιοθέατα, με αποτέλεσμα ένα υψηλό σημείο τήξης (801 ° C).
* ήλιο (He): Ένα ευγενές αέριο με πολύ αδύναμες δυνάμεις διασποράς του Λονδίνου, οδηγώντας σε ένα πολύ χαμηλό σημείο τήξης (-272.2 ° C).
Συνοπτικά: Το σημείο τήξης ενός στερεού αντικατοπτρίζει την ενέργεια που απαιτείται για να ξεπεραστεί οι δυνάμεις που συγκρατούν τα σωματίδια τους. Όσο ισχυρότερη είναι αυτές οι δυνάμεις, τόσο περισσότερη ενέργεια απαιτείται και όσο υψηλότερο είναι το σημείο τήξης.