Πώς μπορεί ένα μόριο να είναι μη πολικό όταν αποτελείται από άτομα που έχουν διαφορετικές ηλεκτροαργασίες;
1. Η μοριακή γεωμετρία έχει σημασία:
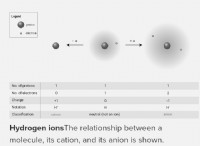
* Ηλεκτροργατιστικότητα Περιγράφει την τάση ενός ατόμου να προσελκύει ηλεκτρόνια σε έναν δεσμό. Όταν τα άτομα με διαφορετικούς δεσμούς ηλεκτροηλεκτρικών περιουσιακών στοιχείων, σχηματίζουν πολικούς ομοιοπολικούς δεσμούς , όπου τα ηλεκτρόνια μοιράζονται άνισα. Αυτό δημιουργεί ένα μερικό αρνητικό φορτίο (δ-) στο πιο ηλεκτροαρνητικό άτομο και ένα μερικό θετικό φορτίο (Δ+) στο λιγότερο ηλεκτροαρνητικό άτομο.
* Μοριακή γεωμετρία είναι η τρισδιάστατη διάταξη των ατόμων σε ένα μόριο. Αυτή η γεωμετρία μπορεί να υπαγορεύσει τον τρόπο με τον οποίο οι πολικότητες των μεμονωμένων δεσμών μέσα σε ένα μόριο αλληλεπιδρούν.
2. Ακύρωση πολικότητας:
* συμμετρικά μόρια: Εάν ένα μόριο έχει συμμετρικό σχήμα και οι πολικοί δεσμοί του είναι διατεταγμένοι συμμετρικά, οι μεμονωμένες πολικότητες των δεσμών μπορούν να ακυρώσουν ο ένας τον άλλον. Αυτό έχει ως αποτέλεσμα ένα μη πολικό μόριο .
* Παράδειγμα: Εξετάστε το διοξείδιο του άνθρακα (CO₂). Το οξυγόνο είναι πιο ηλεκτροαρνητικό από τον άνθρακα, οπότε κάθε δεσμός C =O είναι πολικός. Ωστόσο, το γραμμικό σχήμα του CO₂ σημαίνει ότι οι δύο πολικοί δεσμοί είναι προσανατολισμένοι σε αντίθετες κατευθύνσεις. Οι αντίπαλες πολικότητες ακυρώνουν ο ένας τον άλλον έξω, καθιστώντας το συνολικό μόριο μη πολικό.
3. Άλλοι παράγοντες:
* Διπολικά δίπλωμα: Το μέγεθος της διαφοράς στην ηλεκτροαρνητικότητα μεταξύ των ατόμων επηρεάζει τη δύναμη του διπόλου των δεσμών (μέτρο της πολικότητας ενός δεσμού). Εάν η διαφορά είναι μικρή, ακόμη και με ασύμμετρη διάταξη, το μόριο μπορεί να θεωρηθεί ακόμα μη πολικό.
* Ζεύγη: Μόνο ζεύγη ηλεκτρονίων σε κεντρικό άτομο μπορούν επίσης να συμβάλουν στη μοριακή πολικότητα.
Συνοπτικά:
Ενώ η διαφορά στην ηλεκτροαρνητικότητα μεταξύ των ατόμων σε ένα μόριο δημιουργεί πολικούς δεσμούς, η συνολική πολικότητα του μορίου εξαρτάται από τον τρόπο διατάξεως αυτών των δεσμών στο διάστημα. Οι συμμετρικές ρυθμίσεις μπορούν να οδηγήσουν σε ακύρωση των μεμονωμένων πολικότητας των δεσμών, με αποτέλεσμα ένα μη πολικό μόριο.