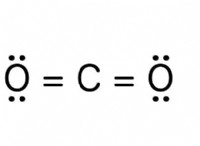Κατά την εξισορρόπηση μιας χημικής εξίσωσης με τι χρειάζονται τα αντιδραστήρια;
Εδώ είναι γιατί:
* Διατήρηση της μάζας: Η θεμελιώδης αρχή πίσω από την εξισορρόπηση των χημικών εξισώσεων είναι ο νόμος της διατήρησης της μάζας. Αυτός ο νόμος δηλώνει ότι η σημασία δεν μπορεί να δημιουργηθεί ή να καταστραφεί σε χημική αντίδραση.
* Άτομα μέσα, άτομα έξω: Για να υποστηρίξει αυτόν τον νόμο, ο ίδιος αριθμός ατόμων κάθε στοιχείου πρέπει να υπάρχει και στις δύο πλευρές της εξίσωσης. Τα αντιδραστήρια είναι τα αρχικά υλικά και τα προϊόντα είναι οι ουσίες που σχηματίζονται ως αποτέλεσμα της αντίδρασης.
Εδώ λειτουργεί:
1. Προσδιορίστε τα στοιχεία: Σημειώστε όλα τα διαφορετικά στοιχεία που υπάρχουν στα αντιδραστήρια και τα προϊόντα.
2. Μετρήστε τα άτομα: Μετρήστε τον αριθμό των ατόμων κάθε στοιχείου και στις δύο πλευρές της εξίσωσης.
3. Ρυθμίστε τους συντελεστές: Χρησιμοποιήστε συντελεστές (αριθμοί μπροστά από τους χημικούς τύπους) για να ρυθμίσετε τον αριθμό των μορίων κάθε αντιδραστηρίου και προϊόντος έως ότου ο αριθμός των ατόμων κάθε στοιχείου είναι ο ίδιος και στις δύο πλευρές.
Παράδειγμα:
Η μη ισορροπημένη εξίσωση για την καύση του μεθανίου είναι:
Ch₄ + o₂ → co₂ + h₂o
Για την εξισορρόπηση αυτής της εξίσωσης:
1. Στοιχεία: Ο άνθρακας (C), το υδρογόνο (Η) και το οξυγόνο (O)
2. Καταμέτρηση: Αντιδραστήρια:1 c, 4 ώρες, 2 o; Προϊόντα:1 c, 2 ώρες, 3 o
3. Εξισορρόπηση:
* Προσθέστε έναν συντελεστή 2 μπροστά από το h₂o:ch₄ + o₂ → co₂ + 2h₂o
* Προσθέστε έναν συντελεστή 2 μπροστά από το o₂:ch₄ + 2o₂ → co₂ + 2h₂o
Τώρα η εξίσωση είναι ισορροπημένη και έχουμε τον ίδιο αριθμό κάθε τύπου ατόμου και στις δύο πλευρές.