Εξηγήστε πώς η ανάπτυξη ατομικών μοντέλων επιδεικνύει επιστημονική διαδικασία;
1. Παρατήρηση και αμφισβήτηση:
* Πρώιμες παρατηρήσεις: Οι άνθρωποι παρατήρησαν τον κόσμο γύρω τους, παρατηρώντας την ύπαρξη διαφορετικών ουσιών, τις ιδιότητές τους και τον τρόπο με τον οποίο αλληλεπιδρούν. Αυτό οδήγησε σε ερωτήσεις σχετικά με τα θεμελιώδη δομικά στοιχεία της ύλης.
* Αρχικά μοντέλα: Οι πρώτοι φιλόσοφοι πρότειναν ιδέες για την ύλη που έγιναν από μικροσκοπικά, αδιαίρετα σωματίδια, τα οποία ονομάζονταν "άτομα" (από την ελληνική λέξη "ατομική" που σημαίνει "ανεκτίμητο").
2. Υπόθεση και Πειραματισμός:
* Ατομική θεωρία του Dalton (1803): Ο John Dalton πρότεινε μια υπόθεση βασισμένη σε πειραματικά στοιχεία. Πρότεινε ότι τα στοιχεία αποτελούνται από πανομοιότυπα άτομα, ότι τα άτομα διαφορετικών στοιχείων είναι διαφορετικά και ότι οι χημικές αντιδράσεις περιλαμβάνουν την αναδιάταξη των ατόμων. Αυτό σημάδεψε μια σημαντική μετατόπιση προς μια πιο επιστημονική προσέγγιση.
* Μοντέλο πουτίγκα του Thomson (1897): J.J. Τα πειράματα της Thomson με ακτίνες καθόδου τον οδήγησαν να ανακαλύψει το ηλεκτρόνιο, ένα αρνητικά φορτισμένο σωματίδιο μέσα στο άτομο. Πρότεινε ένα μοντέλο όπου τα αρνητικά φορτισμένα ηλεκτρόνια ενσωματώθηκαν σε ένα θετικά φορτισμένο "πουτίγκα".
* Πείραμα χρυσού αλουμινίου του Rutherford (1911): Ο Ernest Rutherford πυροβόλησε τα σωματίδια άλφα σε ένα λεπτό χρυσό φύλλο. Παρατήρησε ότι τα περισσότερα σωματίδια περνούσαν κατευθείαν, αλλά μερικά εκτρέπονται, υποδηλώνοντας έναν μικρό, πυκνό, θετικά φορτισμένο πυρήνα στο κέντρο του ατόμου.
3. Θεωρία και βελτίωση:
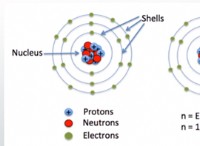
* Πυρηνικό μοντέλο του Rutherford (1911): Με βάση το πείραμά του, ο Rutherford πρότεινε ένα μοντέλο όπου τα ηλεκτρόνια περιστρέφονταν σε ένα μικρό, πυκνό, θετικά φορτισμένο πυρήνα.
* Ατομικό μοντέλο Bohr (1913): Ο Niels Bohr εξέφρασε το μοντέλο του Rutherford, εισάγοντας την έννοια των επιπέδων κβαντισμένων ενεργειακών επιπέδων για τα ηλεκτρόνια, εξηγώντας τα φάσματα γραμμής των στοιχείων.
* Κβαντικό Μηχανικό Μοντέλο (1920S-Present): Αυτό το μοντέλο, που αναπτύχθηκε από τον Schrödinger και άλλα, χρησιμοποιεί μηχανικούς κύματος για να περιγράψει τα ηλεκτρόνια ως σύννεφα πιθανότητας και όχι σε περιστρεφόμενα σωματίδια. Παρέχει μια ακριβέστερη και περίπλοκη περιγραφή του ατόμου.
4. Νέες ερωτήσεις και περαιτέρω έρευνα:
* Κάθε πρόοδος σε ατομικά μοντέλα έθεσε νέες ερωτήσεις και ώθησε περαιτέρω έρευνα. Η ανακάλυψη του νετρονίου (1932) και η ανάπτυξη της φυσικής σωματιδίων οδήγησαν σε ακόμη βαθύτερη κατανόηση της δομής του ατόμου.
* Η αναζήτηση μιας ενοποιημένης θεωρίας για να περιγράψει όλες τις θεμελιώδεις δυνάμεις και σωματίδια συνεχίζεται σήμερα, απεικονίζοντας περαιτέρω την επαναληπτική φύση της επιστημονικής διαδικασίας.
Key Takeaways:
* Επαναληπτική φύση: Η ανάπτυξη ατομικών μοντέλων δεν ήταν μια γραμμική διαδικασία. Περιλάμβανε την οικοδόμηση σε προηγούμενα μοντέλα, την αναθεώρησή τους με βάση νέα στοιχεία και συνεχώς βελτιώνοντας την κατανόησή μας.
* Συνεργασία και οικοδόμηση σε προηγούμενες εργασίες: Πολλοί επιστήμονες συνέβαλαν στην κατανόηση του ατόμου, βασιζόμενοι στο έργο του άλλου και να εξευγενίζουν τις ιδέες τους.
* Σημασία του πειραματισμού: Τα πειραματικά στοιχεία διαδραμάτισαν καθοριστικό ρόλο στη διαμόρφωση και την επικύρωση των ατομικών μοντέλων.
* Συνεχιζόμενη διαδικασία: Η επιστημονική διαδικασία δεν είναι ποτέ πραγματικά "τελειωμένη". Καθώς προκύπτουν νέα στοιχεία, η κατανόησή μας για το άτομο θα συνεχίσει να εξελίσσεται.
Η ιστορία των ατομικών μοντέλων αποτελεί παράδειγμα του τρόπου με τον οποίο η επιστήμη εξελίσσεται μέσω της παρατήρησης, της αμφισβήτησης, της δοκιμής υποθέσεων και της συνεχούς βελτίωσης. Δείχνει τη σημασία της συνεργασίας, τη συλλογιστική που βασίζεται σε αποδεικτικά στοιχεία και τη συνεχή επιδίωξη της γνώσης.