Ποιο μόριο επιταχύνει τις χημικές αντιδράσεις μειώνοντας την ενέργεια ενεργοποίησης;
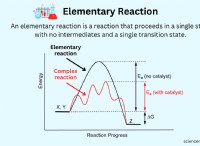
Τα ένζυμα είναι βιολογικοί καταλύτες, που σημαίνει ότι επιταχύνουν τις αντιδράσεις χωρίς να καταναλώνονται στη διαδικασία. Το επιτυγχάνουν αυτό παρέχοντας μια εναλλακτική οδό αντίδρασης με χαμηλότερη ενέργεια ενεργοποίησης, την ελάχιστη ενέργεια που απαιτείται για να συμβεί μια αντίδραση.
Δείτε πώς λειτουργεί:
* Ενεργός ιστότοπος: Τα ένζυμα έχουν μια συγκεκριμένη περιοχή που ονομάζεται ενεργή θέση, η οποία δεσμεύεται με τα αντιδραστήρια (υποστρώματα) της αντίδρασης.
* Ενεργοποίηση ενεργοποίησης: Η ενεργή θέση αλληλεπιδρά με το υπόστρωμα με τρόπο που να στέλνει τους δεσμούς μέσα στο μόριο, καθιστώντας ευκολότερη τη διάσπαση και τη σχηματισμό νέων δεσμών. Αυτό μειώνει την ενέργεια ενεργοποίησης που απαιτείται για να προχωρήσει η αντίδραση.
* Ειδικότητα: Τα ένζυμα είναι ιδιαίτερα συγκεκριμένα, πράγμα που σημαίνει ότι συνήθως καταλύουν μόνο έναν ή μικρό αριθμό αντιδράσεων. Αυτή η εξειδίκευση οφείλεται στο σχήμα και τις χημικές ιδιότητες της ενεργού θέσης.
Παραδείγματα ενζύμων περιλαμβάνουν:
* Λακτάση: Διακόπτει τη λακτόζη (ζάχαρη γάλακτος).
* αμυλάση: Σπάστε το άμυλο σε σάκχαρα.
* πολυμεράση DNA: Κατασκευάζει μόρια ϋΝΑ.
Συνοπτικά, τα ένζυμα είναι απαραίτητα για τη ζωή επειδή επιταχύνουν τις χημικές αντιδράσεις που διαφορετικά θα συνέβαιναν πολύ αργά στη θερμοκρασία του σώματος.