Ο δεσμός Ποιος είναι ο πραγματικός αριθμός ηλεκτρονικών ζεύγους που συνδέονται με ένα ομοιοπολικό δεσμό;
Εδώ είναι γιατί:
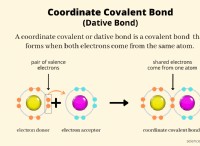
* ομοιοπολικός δεσμός: Ένας ομοιοπολικός δεσμός σχηματίζεται όταν δύο άτομα μοιράζονται ένα ή περισσότερα ζεύγη ηλεκτρονίων.
* Κοινή χρήση ηλεκτρονίων: Κάθε άτομο συνεισφέρει ένα ηλεκτρόνιο στο κοινό ζευγάρι.
* Ζεύγος συγκόλλησης: Αυτό το κοινό ζεύγος ηλεκτρονίων σχηματίζει τον ομοιοπολικό δεσμό και ονομάζεται ζευγάρι συγκόλλησης.
Ας πάρουμε ένα παράδειγμα:
* Μόριο υδρογόνου (H2): Κάθε άτομο υδρογόνου έχει ένα ηλεκτρόνιο. Όταν σχηματίζουν έναν δεσμό, μοιράζονται αυτά τα ηλεκτρόνια, με αποτέλεσμα ένα κοινό ζευγάρι.
* Μόριο νερού (H2O): Το οξυγόνο διαθέτει έξι ηλεκτρόνια σθένους και χρειάζεται δύο ακόμη για να ολοκληρώσει την οκτάδα του. Κάθε άτομο υδρογόνου συνεισφέρει ένα ηλεκτρόνιο, σχηματίζοντας δύο κοινά ζεύγη (ένας δεσμός με κάθε άτομο υδρογόνου).
Επομένως, παρόλο που ένα μόριο μπορεί να έχει πολλαπλούς ομοιοπολικούς δεσμούς (όπως το νερό με δύο), κάθε μεμονωμένος δεσμός αποτελείται πάντα από ένα ζευγάρι κοινόχρηστα ηλεκτρόνια.