Ποιο είναι το pH της αργινίνης;
* Η συγκέντρωση της αργινίνης: Όσο υψηλότερη είναι η συγκέντρωση, τόσο περισσότερο το ρΗ θα επηρεαστεί από τα μόρια αργινίνης.
* Το περιβάλλον περιβάλλον: Το ρΗ του διαλύματος στο οποίο διαλύεται η αργινίνη θα επηρεάσει έντονα την κατάσταση πρωτονίωσης των λειτουργικών ομάδων της.
Εδώ είναι μια πιο λεπτομερής εξήγηση:
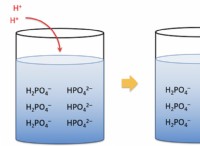
* Η αργινίνη έχει πολλαπλές ιονίζουσες ομάδες: Η αργινίνη έχει τρεις ιονίζουσες ομάδες:μια καρβοξυλική ομάδα (-COOH), μια ομάδα αμινο (-NH2) και μια ομάδα Guanidinium (-c (NH2) 3+). Κάθε ομάδα μπορεί να κερδίσει ή να χάσει ένα πρωτόνιο (Η+), επηρεάζοντας το συνολικό φορτίο του μορίου και του ρΗ του διαλύματος.
* Ισοηλεκτρικό σημείο (PI): Το PI είναι το pH στο οποίο το καθαρό φορτίο του μορίου είναι μηδέν. Για την αργινίνη, το PI είναι περίπου 10,76. Αυτό σημαίνει ότι στο ρΗ 10.76, η αργινίνη υπάρχει στην Zwitterionic μορφή της, όπου τα θετικά και αρνητικά φορτία ισορροπούν.
* pH κάτω από PI: Σε τιμές ρΗ κάτω από το PI, η αργινίνη θα έχει καθαρή θετική φόρτιση επειδή η καρβοξυλική ομάδα της θα είναι πρωτονιωμένη (-COOH), η αμινομάδα της θα είναι πρωτονιωμένη (-NH3+) και η ομάδα του Guanidinium θα παραμείνει θετικά χρεωμένη.
* ph πάνω από PI: Σε τιμές pH πάνω από το PI, η αργινίνη θα έχει καθαρή αρνητική φόρτιση επειδή η καρβοξυλική ομάδα της θα αποπρωτονιωθεί (-COO-), η αμινορή ομάδα της θα αποπρωτονιωθεί (-NH2) και η ομάδα της Guanidinium θα παραμείνει θετικά φορτισμένη.
Για να προσδιορίσετε το ρΗ μιας συγκεκριμένης λύσης αργινίνης, θα πρέπει να γνωρίζετε τη συγκέντρωση της αργινίνης και του ρΗ της διαλύματος που διαλύεται μέσα.
Συνοπτικά:
* Δεν υπάρχει ενιαίο "ph of arginine".
* Το ρΗ της αργινίνης εξαρτάται από τη συγκέντρωσή της και το περιβάλλον.
* Το PI της Arginine είναι 10,76, υποδεικνύοντας το pH στο οποίο υπάρχει ως zwitterion με καθαρό φορτίο μηδέν.