Πώς βοηθά ο καθολικός διαλύτης που ζει;
Εδώ είναι γιατί το νερό είναι απίστευτα σημαντικό για τα ζωντανά πράγματα:
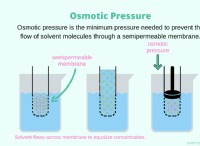
* Εξαιρετικό διαλύτη: Η πολική φύση του νερού του επιτρέπει να διαλύσει μια μεγάλη ποικιλία ουσιών, συμπεριλαμβανομένων των αλάτων, των σάκχαρων και ακόμη και ορισμένων πρωτεϊνών. Αυτό καθιστά ζωτικής σημασίας τη μεταφορά θρεπτικών ουσιών και τη μεταφορά αποβλήτων εντός των οργανισμών.
* Χημικές αντιδράσεις: Πολλές σημαντικές χημικές αντιδράσεις σε ζωντανούς οργανισμούς εμφανίζονται σε υδατικά περιβάλλοντα. Το νερό λειτουργεί ως αντιδραστήριο σε ορισμένες αντιδράσεις και ένα μέσο για τους άλλους.
* Ρύθμιση θερμοκρασίας: Η υψηλή θερμική χωρητικότητα του νερού της επιτρέπει να απορροφά και να απελευθερώνει τη θερμότητα αργά, συμβάλλοντας στη ρύθμιση της θερμοκρασίας του σώματος. Αυτό είναι ιδιαίτερα σημαντικό για τη διατήρηση του λεπτού ισοζυγίου θερμοκρασίας που απαιτείται για τις βιολογικές διεργασίες.
* Λίπανση: Το νερό λειτουργεί ως λιπαντικό, συμβάλλοντας στη μείωση της τριβής μεταξύ των κινούμενων τμημάτων μέσα στο σώμα. Αυτό είναι σημαντικό για πράγματα όπως η κοινή κίνηση και η πέψη.
* Δομική υποστήριξη: Το νερό παρέχει την πίεση του φούρνου, η οποία βοηθά στη διατήρηση του σχήματος των κυττάρων και των ιστών.
Ενώ το νερό είναι ένας εξαιρετικά αποτελεσματικός διαλύτης, δεν διαλύεται απολύτως τα πάντα. Ορισμένες ουσίες, όπως τα λίπη και τα έλαια, είναι υδρόφοβες (απωθημένες από νερό) και απαιτούν από άλλους διαλύτες να διαλύονται.
Συμπερασματικά, το νερό είναι απαραίτητο για τη ζωή λόγω των μοναδικών ιδιοτήτων του, συμπεριλαμβανομένης της ικανότητάς του να διαλύει ένα ευρύ φάσμα ουσιών. Αυτό καθιστά ζωτικής σημασίας για ένα ευρύ φάσμα βιολογικών διεργασιών, από τη μεταφορά θρεπτικών ουσιών έως τη ρύθμιση της θερμοκρασίας.