Ποια είναι η διαφορά μεταξύ των μορίων νερού και του δεσμού μέσα στο μόριο;
Μόρια νερού
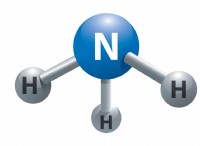
* Ορισμός: Ένα μόριο νερού είναι μια ενιαία μονάδα της ένωσης H₂O. Αποτελείται από δύο άτομα υδρογόνου που συνδέονται με ένα άτομο οξυγόνου.
* Δομή: Το μόριο έχει ένα λυγισμένο σχήμα (όπως ένα V), με το άτομο οξυγόνου στο κέντρο. Η γωνία δεσμού μεταξύ των δύο ατόμων υδρογόνου είναι περίπου 104,5 μοίρες.
* Ιδιότητες: Τα μόρια του νερού είναι πολικά (έχουν ένα ελαφρύ θετικό φορτίο στην πλευρά του υδρογόνου και ένα ελαφρύ αρνητικό φορτίο στην πλευρά του οξυγόνου). Αυτή η πολικότητα οδηγεί σε πολλές από τις μοναδικές ιδιότητες του νερού, όπως η ικανότητά της να διαλύει πολλές ουσίες και να ενεργεί ως καλός διαλύτης.
δεσμοί εντός των μορίων νερού
* Τύπος: Οι δεσμοί που συγκρατούν τα άτομα υδρογόνου και οξυγόνου μαζί σε ένα μόριο νερού είναι ομοιοπολικοί δεσμοί .
* ομοιοπολικός δεσμός: Ένας ομοιοπολικός δεσμός σχηματίζεται όταν δύο άτομα μοιράζονται ηλεκτρόνια. Σε ένα μόριο νερού, κάθε άτομο υδρογόνου μοιράζεται ένα ηλεκτρόνιο με το άτομο οξυγόνου.
* πολικός ομοιοπολικός δεσμός: Οι δεσμοί στο νερό θεωρούνται πολικοί ομοιοπολικοί δεσμοί Επειδή το άτομο οξυγόνου είναι περισσότερο ηλεκτροαρνητικό (προσελκύει ηλεκτρόνια πιο έντονα) από τα άτομα υδρογόνου. Αυτή η ανομοιόμορφη κατανομή των ηλεκτρονίων δημιουργεί τις μερικές θετικές και αρνητικές χρεώσεις στο μόριο.
Συνοπτικά:
* Μόρια νερού είναι οι μεμονωμένες μονάδες του νερού ουσίας (H₂O).
* δεσμούς μέσα στα μόρια είναι οι δυνάμεις που συγκρατούν τα άτομα μαζί μέσα σε ένα μόνο μόριο νερού. Αυτοί οι δεσμοί είναι ειδικά ομοιοπολικοί δεσμοί, οι οποίοι περιλαμβάνουν την ανταλλαγή ηλεκτρονίων.
Επιτρέψτε μου να ξέρω αν θέλετε μια πιο λεπτομερή εξήγηση για οποιαδήποτε από αυτές τις έννοιες!