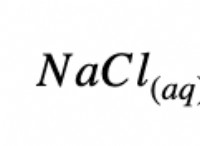Πώς διαλύει το νερό θρεπτικά συστατικά;
1. Πολικότητα: Το νερό είναι ένα πολικό μόριο, που σημαίνει ότι έχει ένα ελαφρώς θετικό τέλος και ένα ελαφρώς αρνητικό τέλος. Αυτό οφείλεται στην άνιση κατανομή των ηλεκτρονίων μεταξύ των ατόμων υδρογόνου και οξυγόνου στο μόριο του νερού.
2. Ιδιότητες θρεπτικών ουσιών: Πολλά θρεπτικά συστατικά, όπως τα σάκχαρα, τα άλατα και τα αμινοξέα, είναι επίσης πολικά μόρια ή ιοντικές ενώσεις. Αυτές οι ουσίες έχουν χρεώσει περιοχές ή μερικές χρεώσεις.
3. Αλληλεπίδραση: Όταν το νερό συναντά αυτά τα πολικά θρεπτικά συστατικά, το θετικό τέλος του μορίου νερού προσελκύει το αρνητικό άκρο του θρεπτικού μορίου και αντίστροφα. Αυτές οι ηλεκτροστατικές αλληλεπιδράσεις δημιουργούν μια δύναμη που τραβά τα θρεπτικά μόρια χωριστά και τα περιβάλλει με μόρια νερού, διαλύοντας τους αποτελεσματικά.
4. Κοσμήματα ενυδάτωσης: Τα μόρια του νερού σχηματίζουν ένα "κέλυφος ενυδάτωσης" γύρω από τα διαλυμένα θρεπτικά μόρια, διατηρώντας τα χωρισμένα και διασκορπισμένα μέσα στο νερό.
Εδώ είναι ένα συγκεκριμένο παράδειγμα:
* αλάτι (NaCl): Το αλάτι είναι μια ιοντική ένωση με θετικά φορτισμένα ιόντα νατρίου (Na+) και αρνητικά φορτισμένα ιόντα χλωριούχου (Cl-). Τα μόρια του νερού περιβάλλουν τα ιόντα, με τα θετικά άκρα των μορίων του νερού να προσελκύονται από τα ιόντα χλωριδίου και τα αρνητικά άκρα που προσελκύονται από τα ιόντα νατρίου. Αυτή η αλληλεπίδραση σπάει τους ιοντικούς δεσμούς που κρατούν το αλάτι μαζί, διαλύοντας το στο νερό.
Η διαδικασία διάλυσης των θρεπτικών ουσιών στο νερό είναι απαραίτητη για:
* Απορρόφηση: Επιτρέπει τη ληφθείσα θρεπτικά συστατικά από τα κύτταρα του σώματος.
* Μεταφορά: Δίνει τη δυνατότητα στα θρεπτικά συστατικά να ταξιδεύουν σε όλο το σώμα μέσω της κυκλοφορίας του αίματος.
* Χημικές αντιδράσεις: Πολλές βιολογικές αντιδράσεις εμφανίζονται στο νερό και τα διαλυμένα θρεπτικά συστατικά είναι απαραίτητα για την πραγματοποίηση αυτών των αντιδράσεων.
Δεν διαλύονται όλα τα θρεπτικά συστατικά στο νερό:
* Ορισμένα θρεπτικά συστατικά, όπως τα λίπη και τα έλαια, είναι μη πολικά και δεν διαλύονται εύκολα στο νερό. Απαιτούν άλλους μηχανισμούς όπως η γαλακτωματοποίηση (καταρρίπτοντας σε μικρότερα σταγονίδια) για να αφομοιωθούν και να απορροφηθούν.