Γιατί το οξύ που κάνει ασβεστόλιθο fizz μια χημική αλλαγή;
* Δημιουργούνται νέες ουσίες: Όταν το οξύ αντιδρά με ασβεστόλιθο (ανθρακικό ασβέστιο), παράγει νέες ουσίες:
* αέριο διοξειδίου του άνθρακα: Αυτό είναι το αέριο που προκαλεί την ανατροπή.
* αλάτι: Το συγκεκριμένο άλας εξαρτάται από το χρησιμοποιούμενο οξύ. Για παράδειγμα, με υδροχλωρικό οξύ, παίρνετε χλωριούχο ασβέστιο.
* νερό: Η αντίδραση απελευθερώνει επίσης νερό.
* μη αναστρέψιμη αλλαγή: Οι αρχικές ουσίες (ασβεστόλιθος και οξύ) μετασχηματίζονται σε εντελώς διαφορετικές ουσίες. Δεν μπορείτε εύκολα να πάρετε το ασβεστόλιθο και το οξύ πίσω.
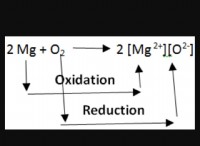
* Χημικοί δεσμοί Break and Form: Η αντίδραση περιλαμβάνει το σπάσιμο των χημικών δεσμών στον ασβεστόλιθο και το οξύ και τον σχηματισμό νέων δεσμών για τη δημιουργία των προϊόντων.
Η χημική εξίσωση:
Η αντίδραση του υδροχλωρικού οξέος (HCl) με ασβεστόλιθο (CACO3) μπορεί να αναπαρασταθεί από την ακόλουθη εξίσωση:
2HCL (aq) + caCO3 (s) → CaCl2 (aq) + H2O (L) + CO2 (g)
* (aq) υποδεικνύει ότι η ουσία διαλύεται σε νερό (υδατικό διάλυμα).
* (s) υποδεικνύει ένα στερεό.
* (l) υποδεικνύει υγρό.
* (g) υποδεικνύει ένα αέριο.
Συνοπτικά: Η ανατροπή που βλέπετε όταν το οξύ αντιδρά με ασβεστόλιθο είναι αποτέλεσμα μιας χημικής αλλαγής όπου σχηματίζονται νέες ουσίες, οι αρχικές ουσίες καταναλώνονται και οι χημικοί δεσμοί σπάζουν και σχηματίζονται.