Ποια είναι τα παραδείγματα στερεάς ένωσης;
Ιωνικές ενώσεις:
* Χλωριούχο νάτριο (NaCl): Πίνακας αλάτι, μια πολύ κοινή ένωση.
* ανθρακικό ασβέστιο (CACO3): Βρέθηκαν σε ασβεστόλιθο, κιμωλία και κοχύλια.
* οξείδιο μαγνησίου (MGO): Που χρησιμοποιούνται σε διάφορες βιομηχανικές εφαρμογές.
* ιωδιούχο κάλιο (KI): Βρέθηκε σε ιωδιούχο αλάτι και χρησιμοποιήθηκε στην ιατρική.
* Θειικό χαλκό (CUSO4): Ένα μπλε κρυσταλλικό στερεό που χρησιμοποιείται σε λιπάσματα και φυτοφάρμακα.
ομοιοπολικές ενώσεις:
* ζάχαρη (C12H22O11): Ένα κοινό γλυκαντικό.
* νερό (H2O): Ο πάγος είναι η στερεή μορφή νερού.
* διοξείδιο του άνθρακα (CO2): Ο ξηρός πάγος είναι η στερεή μορφή διοξειδίου του άνθρακα.
* διοξείδιο του πυριτίου (SiO2): Βρέθηκε σε άμμο, χαλαζία και γυαλί.
* Diamond (C): Μια πολύ σκληρή και πολύτιμη μορφή άνθρακα.
Μεταλλικές ενώσεις:
* IRON (FE): Ένα κοινό μέταλλο που χρησιμοποιείται στην κατασκευή και την κατασκευή.
* Χαλκός (Cu): Χρησιμοποιείται στην καλωδίωση και τις υδραυλικές εγκαταστάσεις.
* αλουμίνιο (al): Ένα ελαφρύ μέταλλο που χρησιμοποιείται σε δοχεία αεροσκαφών και ποτών.
* χρυσό (AU): Ένα πολύτιμο μέταλλο που χρησιμοποιείται σε κοσμήματα και ηλεκτρονικά.
* ασήμι (AG): Ένα άλλο πολύτιμο μέταλλο που χρησιμοποιείται σε κοσμήματα και φωτογραφία.
Άλλες στερεές ενώσεις:
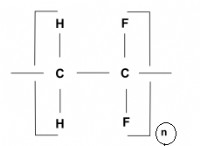
* Πολυμερή: Μεγάλα μόρια που σχηματίζονται από επαναλαμβανόμενες μονάδες, όπως το πολυαιθυλένιο (πλαστικό).
* κεραμικά: Ανόργανα υλικά όπως η πορσελάνη και τα τούβλα.
* σύνθετα υλικά: Υλικά από δύο ή περισσότερα διαφορετικά υλικά, όπως το υαλοβάμβακα.
Αυτός ο κατάλογος δεν είναι εξαντλητικός, αλλά παρέχει ένα καλό σημείο εκκίνησης για να κατανοήσουμε τη διαφορετική φύση των στερεών ενώσεων.