Μπορούν οι ενώσεις να υποβληθούν σε χημική αλλαγή για να γίνουν στοιχεία;
* Τα στοιχεία είναι τα θεμελιώδη δομικά στοιχεία της ύλης. Δεν μπορούν να αναλυθούν σε απλούστερες ουσίες με συνηθισμένα χημικά μέσα.
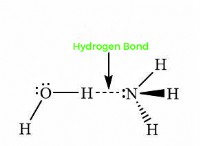
* Οι ενώσεις σχηματίζονται από τον χημικό συνδυασμό δύο ή περισσότερων στοιχείων σε σταθερή αναλογία Για παράδειγμα, το νερό (H₂O) είναι μια ένωση που σχηματίζεται από τα στοιχεία υδρογόνου και οξυγόνου.
Για να σπάσει μια ένωση κάτω στα συστατικά της στοιχεία, χρειάζεστε μια χημική αντίδραση που περιλαμβάνει τη διάσπαση των χημικών δεσμών που συγκρατούν τα στοιχεία. Αυτό επιτυγχάνεται συνήθως μέσω διαδικασιών όπως:
* ηλεκτρόλυση: Χρησιμοποιώντας ηλεκτρική ενέργεια για την αποσύνθεση μιας ένωσης, όπως η διάσπαση του νερού σε υδρογόνο και οξυγόνο.
* αντιδράσεις αποσύνθεσης: Η διάσπαση μιας ένωσης με θέρμανση ή χρησιμοποιώντας έναν καταλύτη, όπως η αποσύνθεση του ανθρακικού ασβεστίου (CACO₃) σε οξείδιο του ασβεστίου (CAO) και διοξείδιο του άνθρακα (CO₂).
Στην ουσία, οι χημικές αλλαγές μπορούν να αναδιατάξουν τα άτομα μέσα σε μια ένωση, αλλά δεν μπορούν να δημιουργήσουν ή να καταστρέψουν στοιχεία.