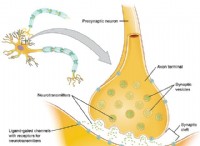
Πώς είναι η λύση και το μόριο το ίδιο;
μόριο:
* Ορισμός: Μια ομάδα δύο ή περισσότερων ατόμων που συγκρατούνται από χημικούς δεσμούς.
* Παράδειγμα: Το νερό (H₂O) είναι ένα μόριο που αποτελείται από δύο άτομα υδρογόνου και ένα άτομο οξυγόνου.
* Focus: Δομή και σύνθεση μεμονωμένων μονάδων.
Λύση:
* Ορισμός: Ένα ομοιογενές μίγμα δύο ή περισσοτέρων ουσιών.
* Παράδειγμα: Το αλμυρό νερό είναι ένα διάλυμα όπου το αλάτι (διαλυμένη ουσία) διαλύεται σε νερό (διαλύτης).
* Focus: Η ομοιόμορφη κατανομή μιας ουσίας μέσα σε μια άλλη.
Σχέση:
* Τα μόρια μπορούν να είναι συστατικά των λύσεων: Η διαλυμένη ουσία σε ένα διάλυμα αποτελείται συχνά από μεμονωμένα μόρια που διασκορπίζονται σε όλο τον διαλύτη.
* Οι λύσεις μπορούν να αποτελούνται από διαφορετικούς τύπους μορίων: Ένα διάλυμα μπορεί να περιέχει πολλαπλούς τύπους μορίων, όπως τα διαφορετικά μόρια σε διάλυμα ζάχαρης-νερού.
Συνοπτικά: Ένα μόριο είναι ένα θεμελιώδες δομικό στοιχείο, ενώ μια λύση είναι ένα μεγαλύτερο σύστημα που μπορεί να αποτελείται από πολλά διαφορετικά μόρια.