Γιατί τα αντιδραστήρια χρησιμοποιούνται για τη δοκιμή για τα κατιόντα συνήθως αλκαλικά μεταλλικά άλατα ή αμμώνιο και όχι για άλλα μέταλλα;
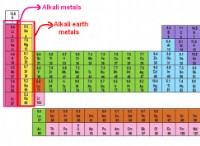
* Αλκαλικά μέταλλα (Li, na, k, rb, cs) και αμμώνιο (NH₄⁺) Form Διαλυτά άλατα με τα περισσότερα ανιόντα . Αυτό σημαίνει ότι τα κατιόντα τους είναι θεατές ιόντα Στην αντίδραση, που σημαίνει ότι δεν συμμετέχουν ενεργά στην αντίδραση που σχηματίζει το ίζημα ή την αλλαγή χρώματος που παρατηρείτε.
* Άλλα μέταλλα Συχνά σχηματίζουν αδιάλυτα άλατα με διάφορα ανιόντα. Εάν χρησιμοποιείτε ένα αντιδραστήριο που περιέχει ένα κατιόν από άλλο μέταλλο, μπορείτε να πάρετε ένα ψευδώς θετικό Εάν αυτό το μέταλλο σχηματίζει ένα αδιάλυτο αλάτι με το ανιόν που προσπαθείτε να δοκιμάσετε. Αυτό θα έσφιξε τα αποτελέσματά σας και θα δυσκολεύει να διαπιστωθεί εάν το ίζημα σχηματίζεται λόγω του κατιόντος που δοκιμάζετε για ή λόγω του κατιόντος στο αντιδραστήριο σας.
Εδώ είναι ένα απλό παράδειγμα:
Φανταστείτε ότι θέλετε να δοκιμάσετε την παρουσία ιόντων αργύρου (AG⁺) χρησιμοποιώντας ένα αντιδραστήριο.
* Εάν χρησιμοποιείτε χλωριούχο νάτριο (NaCl), τα ιόντα νατρίου (Na⁺) θα είναι ιόντα θεατών. Η αντίδραση θα είναι:
Ag⁺ + CL⁻ → AgCl (S) (το χλωριούχο ασήμι είναι αδιάλυτο, σχηματίζοντας λευκό ίζημα)
* Εάν χρησιμοποιείτε χλωριούχο χαλκού (CuCl₂), τα ιόντα χαλκού (Cu2⁺) θα μπορούσαν επίσης να αντιδράσουν με τα ιόντα χλωριούχου και να σχηματίζουν χλωριούχο χαλκό (Cucl₂), το οποίο είναι διαλυτό. Αυτό θα δημιουργούσε ένα σύγχρονο αποτέλεσμα, καθιστώντας δύσκολη την αναφορά εάν το ίζημα οφείλεται σε ιόντα αργύρου ή ιόντα χαλκού.
Συνοπτικά:
Τα αλκαλικά μεταλλικά άλατα και τα άλατα αμμωνίου χρησιμοποιούνται ως αντιδραστήρια επειδή είναι:
* πολύ διαλυτό :Δεν θα παρεμβαίνουν στις αντιδράσεις που προσπαθείτε να παρατηρήσετε.
* ιόντα θεατών :Δεν συμβάλλουν στο σχηματισμό ιζημάτων ή αλλαγών χρώματος, καθιστώντας τα αποτελέσματα ευκολότερα στην ερμηνεία.
Αυτό εξασφαλίζει ότι οι παρατηρούμενες αντιδράσεις οφείλονται στην αλληλεπίδραση του κατιόντος που δοκιμάζετε με το αντιδραστήριο, παρέχοντας ακριβή και αξιόπιστα αποτελέσματα.