Γιατί το όξινο χλωριούχο βηρύλλιο στο νερό;
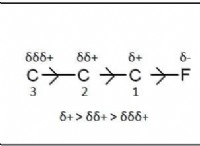
1. Πόλωση του δεσμού και της υδρόλυσης BE-CL:
* Το Beryllium είναι ένα μικρό, εξαιρετικά φορτισμένο κατιόν (BE²⁺). Αυτό καθιστά τον δεσμό BE-CL εξαιρετικά πολικό, με σημαντικό θετικό φορτίο στο άτομο βηρυλλίου και αρνητικό φορτίο στα άτομα χλωρίου.
* Όταν ο Becl₂ διαλύεται σε νερό, ο πολωμένος δεσμός BE-CL αποδυναμώνει, επιτρέποντας στα μόρια του νερού να επιτεθούν στο άτομο βηρύλλου.
* Αυτό οδηγεί σε υδρόλυση , όπου ένα μόριο νερού διασπάται, με ένα ιόν υδρογόνου (Η) να συνδέεται με το ιόν χλωριδίου και το ιόν υδροξειδίου (OH⁻) που συνδέεται με το άτομο βηρυλλίου.
2. Σχηματισμός όξινων διαλυμάτων:
* Η αντίδραση υδρόλυσης παράγει υδροξείδιο του βηρυλλίου [ΒΕ (ΟΗ) ₂] και υδροχλωρικό οξύ (HCl) .
* Το υδροξείδιο του βηρυλλίου είναι μια αδύναμη βάση, αλλά αντιδρά εύκολα με νερό για να σχηματίσει περισσότερα ιόντα Η, αυξάνοντας περαιτέρω την οξύτητα του διαλύματος.
* Το HCl που παράγεται είναι ένα ισχυρό οξύ, το οποίο συμβάλλει επίσης σημαντικά στην όξινη φύση του διαλύματος.
Συνολική αντίδραση:
Beckl₂ (aq) + 2 h₂o (l) ⇌ be (oh) ₂ (aq) + 2 hcl (aq)
Συνοπτικά: Ο συνδυασμός του εξαιρετικά πολικού δεσμού BE-CL, της υδρόλυσης και του σχηματισμού ισχυρού οξέος (HCl) και μιας αδύναμης βάσης (BE (OH) ₂) που αντιδρά περαιτέρω με νερό για την παραγωγή ιόντων Η, έχει ως αποτέλεσμα το χλωριούχο βηρύλλιο να είναι όξινο στο νερό.