Τύποι επαγωγικών επιδράσεων
Όταν το ζεύγος δεσμών κινείται προς το πιο ηλεκτραρνητικό άτομο, πολώνει έναν δεσμό σίγμα. Η πόλωση συμβαίνει μεταξύ δύο ατόμων με ποικίλη ηλεκτραρνητικότητα. Το ηλεκτραρνητικό άτομο λαμβάνει μόνο ένα μερικό αρνητικό φορτίο, ενώ το άλλο άτομο λαμβάνει ένα μερικό θετικό φορτίο.
Η επαγόμενη πολικότητα μεταδίδεται στους δεσμούς σίγμα του μορίου, σχηματίζοντας ένα μόνιμο δίπολο. Αυτή η μετάδοση φορτίων από το ένα άτομο στο άλλο ονομάζεται επαγωγικό φαινόμενο. Αυτό το άρθρο εξετάζει το επαγωγικό αποτέλεσμα και τον ορισμό του, παραδείγματα και τη σειρά του.
Τι είναι το επαγωγικό αποτέλεσμα;
Σε έναν ομοιοπολικό δεσμό σ μεταξύ δύο ατόμων μεταβαλλόμενης ηλεκτραρνητικότητας, το πιο ηλεκτραρνητικό άτομο έλκει το ζεύγος δεσμού επειδή έχει πολύ μεγαλύτερη συγγένεια με τα ηλεκτρόνια. Λόγω αυτής της έλξης, περισσότερα ηλεκτραρνητικά άτομα παράγουν ένα μερικό αρνητικό φορτίο (σ –), ενώ το άλλο αναπτύσσει ένα μερικό θετικό φορτίο (σ+). Αυτή η διαδικασία οδηγεί σε άνιση κατανομή του ηλεκτρονίου σύνδεσης.
Ο ομοιοπολικός δεσμός πολώνεται, σχηματίζοντας ένα μόνιμο δίπολο στον δεσμό. Το επαγωγικό αποτέλεσμα αναφέρεται στη συνεχή κατάσταση πόλωσης δεσμού. Το σύμβολο για το επαγωγικό αποτέλεσμα είναι (–>–), με το βέλος. Το βέλος δείχνει πάντα προς το πιο ηλεκτραρνητικό άτομο.

Το επαγωγικό φαινόμενο περνά από το ένα άτομο στο επόμενο άτομο με τη μορφή μιας ένωσης μακράς αλυσίδας. Αλλά το αποτέλεσμα σταδιακά εξασθενεί και γίνεται ασήμαντο. Για παράδειγμα, ας υποθέσουμε ότι το τερματικό ενός ατόμου άνθρακα είναι συζευγμένο με ένα ηλεκτραρνητικό άτομο αλογόνου (ομάδα απόσυρσης ηλεκτρονίων). Σε μια τέτοια περίπτωση, το θετικό φορτίο περνά σε όλη την ανθρακική αλυσίδα. Αυτό το επαγωγικό αποτέλεσμα φαίνεται στο διάγραμμα.
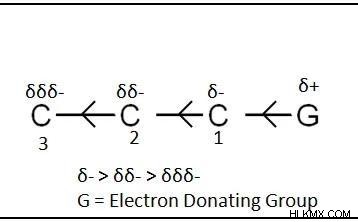
Παρόμοια με το επαγωγικό φαινόμενο, όταν μια ομάδα ή άτομο που δίνει ηλεκτρόνια συνδέεται με το τερματικό άτομο άνθρακα μιας ανθρακικής αλυσίδας, το αρνητικό φορτίο περνά στην ανθρακική αλυσίδα, όπως φαίνεται στο διάγραμμα.
Διαφορετικοί τύποι επαγωγικού αποτελέσματος
+I Effect
Όταν ένα άτομο ή ομάδα συνεισφέρει ηλεκτρόνια στο σχηματισμό ενός δεσμού και αποκτά μερικό θετικό φορτίο, ανήκει στην ομάδα +I. Εδώ το αποτέλεσμα ονομάζεται θετικό επαγωγικό αποτέλεσμα ή φαινόμενο +I. Ας προσπαθήσουμε να κατανοήσουμε τους τύπους επαγωγικών εφέ.
Παράδειγμα ομάδων +I:
– O –, – COO –, –CR3, –CHR2, – CH2R, –CH3, –D
-Εφέ
Η ομάδα -I σχηματίζεται όταν ένα άτομο ή ομάδα προσελκύει συνδετικά ηλεκτρόνια προς τον εαυτό του και συσσωρεύει ένα μερικό αρνητικό φορτίο. Αυτό το φαινόμενο ονομάζεται επίσης επαγωγικό φαινόμενο απόσυρσης ηλεκτρονίων ή φαινόμενο -I.
Παράδειγμα ομάδων -I:
–NO2, – SO2R, –CN, –SO2Ar, –COOH, –F, – Cl, – Br, – I, –OAr, –COOR, –OR, –COR, –SH, –SR, –OH, –Ar, – CH =CR2
Τι είναι η σειρά επαγωγικού αποτελέσματος;
Για επαγωγικά εφέ – I και + I, μπορούν να οριστούν οι ακόλουθες ομάδες κατά σειρά φθίνουσας ισχύος:
Επαγωγική σειρά εφέ για ομάδες +I
– O –> – COO –> –CR3> –CHR2> – CH2R> –CH3> –D
Επαγωγική σειρά εφέ για ομάδες -I
-NR3+> -SR2+> -NH3+> –NO3> – SO2R> –CN> –SO2Ar> –COOH> –F> – Cl> – Br> – I> –OAr> –COOR> –OR> –COR> –SH> –SR> –OH> –Ar> – CH =CR2
Ποια είναι μερικά χαρακτηριστικά του επαγωγικού εφέ;
Το επαγωγικό φαινόμενο προκύπτει λόγω διαφορών στην ηλεκτραρνητικότητα που προκαλούνται από δύο άτομα που είναι δεσμοί σίγμα ( σ).
Το επαγωγικό αποτέλεσμα μεταφέρεται στους δεσμούς σίγμα, δεν υπάρχει μέρος των δεσμών pi (π)
Εάν απομακρυνθείτε από τις ομάδες που το προκαλούν, το εύρος του επαγωγικού αποτελέσματος θα μειωθεί επίσης
Το επαγωγικό αποτέλεσμα διαρκεί για μεγάλο χρονικό διάστημα, έχει επίσης τη δυνατότητα να σχηματίσει ένα επίμονο δίπολο στο μόριο
Αυτό το φαινόμενο είναι αδύναμο και μερικές φορές υπερισχύεται από άλλες διεργασίες ηλεκτρονίων όπως συντονισμός, υπερσύζευξη κ.λπ.
Οι επαγωγικές επιδράσεις επηρεάζουν τις ουσίες τόσο χημικά όσο και φυσικά
Ποια είναι η χρήση του επαγωγικού αποτελέσματος;
Το επαγωγικό αποτέλεσμα επηρεάζει ορισμένες κρίσιμες ιδιότητες των οργανικών ενώσεων. Μερικά από αυτά μπορεί να περιλαμβάνουν:
Προσδιορισμός της όξινης ισχύος των αλειφατικών καρβοξυλικών οξέων
Η αξιολόγηση της σταθερότητας του καρβοκατιόντος αλκυλίου, των καρβανιόντων και των ριζών χωρίς άνθρακα εξαρτάται επίσης από επαγωγικά αποτελέσματα
Επηρεάζει τη διπολική ροπή και το μήκος δεσμού
Το επαγωγικό αποτέλεσμα επηρεάζει την αντοχή των οργανικών βάσεων
1. Σταθερότητα καρβοκατιόν (ιόντα άνθρακα)
Όταν ομάδες +I όπως το αλκύλιο υπάρχουν δίπλα στον θετικά φορτισμένο άνθρακα, η σταθερότητα του καρβοκατιόντος θα αυξηθεί. Χρησιμοποιώντας το θετικό επαγωγικό αποτέλεσμα, οι ομάδες +I θα βοηθήσουν στη μείωση του θετικού φορτίου στον άνθρακα δίνοντας μια αρνητική πυκνότητα φορτίου. Εξαιτίας αυτού, το καρβοκατιόν θα γίνει σταθερό.
Οι ομάδες -I θα αποσταθεροποιήσουν επίσης το καρβοκατιόν. Θα αυξήσει το θετικό φορτίο αφαιρώντας την πυκνότητα των ηλεκτρονίων. Μπορείτε να δείτε ότι κάθε παράγοντας που βοηθά στην αύξηση του φορτίου, είτε θετικός είτε αρνητικός, σε ένα ιόν προκαλεί αποσταθεροποίηση. Ταυτόχρονα, οποιοσδήποτε παράγοντας μειώνει τη φόρτιση προκαλεί τη σταθεροποίησή της.
Η σειρά σταθερότητας των καρβοκατιόντων με το αλκύλιο, για παράδειγμα, φαίνεται παρακάτω:
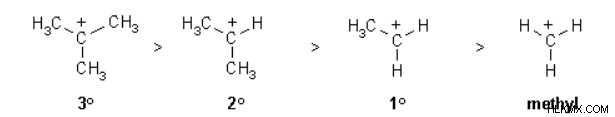
Εάν το καρβοκατιόν έχει δύο αλκυλομάδες, είναι πιο σταθερό από το πρωτογενές καρβοκατιόν και το τριτοταγές καρβοκατιόν με τρεις αλκυλομάδες. Αν εξετάσουμε όλες αυτές τις επιλογές, το μεθυλοκαρβοκατιόν είναι το λιγότερο σταθερό.
2. Σταθερότητα ελεύθερων ριζών:
Η σταθερότητα των ελεύθερων ριζών θα αυξηθεί λόγω των αυξημένων αλκυλομάδων. Η σταθερότητα των διαφόρων ελεύθερων ριζών φαίνεται στο παρακάτω παράδειγμα:
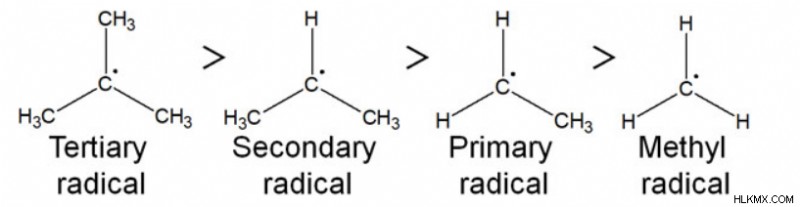
2. Σταθερότητα Carbanions:
Οι ομάδες +I έχουν χαμηλότερη σταθερότητα ανθρακικού, ενώ οι ομάδες -I βοηθούν στην αύξησή τους. Οι ομάδες αλκυλίου (+Ι), για παράδειγμα, θα μεταφέρουν την πυκνότητα των ηλεκτρονίων στον αρνητικά φορτισμένο άνθρακα, αυξάνοντας έτσι την αστάθεια του καρβανίου. Λόγω αυτού, τα ανθρακώματα είναι σταθερά με την ακόλουθη σειρά:
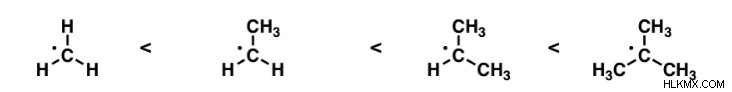
Συμπέρασμα
Το επαγωγικό φαινόμενο είναι το φαινόμενο κατά το οποίο σχηματίζεται ένα μόνιμο δίπολο σε ένα δεδομένο μόριο λόγω άνισου δεσμού κοινής χρήσης ηλεκτρονίων. Δημιουργεί επίσης μια πολωμένη κατάσταση που διαρκεί περισσότερο. Θα υπάρχουν δύο ανόμοια άτομα σε έναν δεσμό σίγμα και η πυκνότητα των ηλεκτρονίων επίσης δεν θα είναι ομοιόμορφη. Οι επαγωγικές επιδράσεις επηρεάζουν τις ουσίες τόσο χημικά όσο και φυσικά. Επηρεάζει ορισμένες κρίσιμες ιδιότητες των οργανικών ενώσεων. Μπορεί να χρησιμοποιηθεί για τον προσδιορισμό της όξινης ισχύος των αλειφατικών καρβοξυλικών οξέων, την αξιολόγηση της σταθερότητας του καρβοκατιόντος αλκυλίου, των καρβανιόντων και των ριζών ελεύθερων άνθρακα, της διπολικής ροπής και του μήκους δεσμού και της αντοχής των οργανικών βάσεων, μεταξύ άλλων.