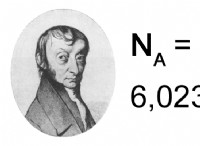Πόσο εύκολα μπορεί να διαλυθεί μια ουσία σε υγρό;
Παράγοντες που επηρεάζουν τη διαλυτότητα:
* Φύση της διαλυμένης ουσίας και του διαλύτη:
* "Όπως διαλύεται όπως": Οι πολικές διαλυμένες ουσίες (όπως η ζάχαρη) διαλύονται καλά σε πολικούς διαλύτες (όπως το νερό), ενώ οι μη πολικές διαλυμένες ουσίες (όπως το πετρέλαιο) διαλύονται καλά σε μη πολικούς διαλύτες (όπως η βενζίνη).
* Θερμοκρασία: Γενικά, η αύξηση της θερμοκρασίας αυξάνει τη διαλυτότητα για στερεά και αέρια. Ωστόσο, υπάρχουν εξαιρέσεις, όπως η διαλυτότητα των αερίων που μειώνονται με την αύξηση της θερμοκρασίας.
* Πίεση: Για τα αέρια, η αύξηση της πίεσης αυξάνει τη διαλυτότητα.
* Μέγεθος σωματιδίων: Τα μικρότερα σωματίδια διαλύονται ταχύτερα από τα μεγαλύτερα επειδή έχουν μεγαλύτερη επιφάνεια που εκτίθεται στον διαλύτη.
* ανάδευση ή αναταραχή: Η ανάμειξη επιταχύνει τη διαδικασία διάλυσης φέρνοντας σε επαφή με το φρέσκο διαλύτη με τη διαλυμένη ουσία.
Διαλυτότητα μέτρησης:
Η διαλυτότητα εκφράζεται συνήθως ως η συγκέντρωση της διαλελυμένης ουσίας σε ένα κορεσμένο διάλυμα, το οποίο είναι ένα διάλυμα που δεν μπορεί να διαλύσει οποιαδήποτε διαλυμένη ουσία σε μια δεδομένη θερμοκρασία και πίεση. Οι κοινές μονάδες για τη διαλυτότητα περιλαμβάνουν:
* γραμμάρια ανά 100 γραμμάρια διαλύτη (g/100g)
* moles ανά λίτρο διαλύτη (mol/L)
"Εύκολα" είναι σχετικό:
Δεν υπάρχει απόλυτη κλίμακα για την "εύκολη" διάλυση. Ορισμένες ουσίες, όπως το αλάτι στο νερό, διαλύονται εύκολα, ενώ άλλες, όπως η άμμος στο νερό, διαλύονται σχεδόν καθόλου. Ο όρος "εύκολα" εξαρτάται από το πλαίσιο και τις συγκεκριμένες ουσίες.
Συνοπτικά, η διαλυτότητα είναι μια πολύπλοκη ιδιότητα που επηρεάζεται από διάφορους παράγοντες και εξαρτάται από τις συγκεκριμένες ουσίες και τις συνθήκες.