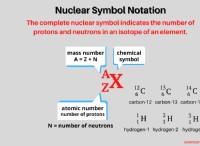
Ποιο στοιχείο έχουν τα περισσότερα από τα πολυατομικά ιόντα στη φόρμουλα;
Εδώ είναι γιατί:
* Υψηλή ηλεκτροαρνητικότητα: Το οξυγόνο είναι εξαιρετικά ηλεκτροαρνητικό, που σημαίνει ότι προσελκύει έντονα ηλεκτρόνια. Αυτό το καθιστά καλό υποψήφιο για τη διαμόρφωση ιοντικών δεσμών με άλλα στοιχεία.
* Δυνατότητα σχηματισμού πολλαπλών δεσμών: Το οξυγόνο μπορεί να σχηματίσει διπλούς και ακόμη και τριπλούς δεσμούς, επιτρέποντάς του να συμμετέχει σε σύνθετα πολυατομικά ιόντα.
* αφθονία: Το οξυγόνο είναι το πιο άφθονο στοιχείο στην κρούστα της Γης, καθιστώντας το άμεσα διαθέσιμο για τη διαμόρφωση ενώσεων.
Παραδείγματα κοινών πολυατομικών ιόντων που περιέχουν οξυγόνο περιλαμβάνουν:
* θειικό άλας (so₄²⁻)
* νιτρικά (no₃⁻)
* ανθρακικό (co₃²)
* φωσφορικό (po₄³⁻)
* Υδροξείδιο (OH⁻)
Ενώ υπάρχουν μερικά πολυατομικά ιόντα χωρίς οξυγόνο (όπως το αμμόνιο (NH₄⁺)), η πλειοψηφία από αυτά περιέχει οξυγόνο.