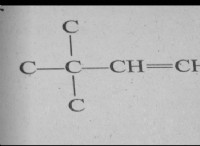
Ποιο από τα δύο από τα δύο O2NCH2CH2O- ή CHCH2O- αναμένεται να είναι πιο σταθερά και γιατί;
* Εφέ με την εξαγωγή ηλεκτρονίων της ομάδας NITRO: Η ομάδα NITRO (-NO2) είναι μια ισχυρή ομάδα ηλεκτρονίων-μελαγχολικά. Αυτό σημαίνει ότι τραβάει πυκνότητα ηλεκτρονίων μακριά από το υπόλοιπο μόριο. Στο `O2NCH2CH2O -`, η ομάδα Nitro τραβά την πυκνότητα ηλεκτρονίων από το αρνητικά φορτισμένο άτομο οξυγόνου, βοηθώντας στη σταθεροποίηση του αρνητικού φορτίου.
* σταθεροποίηση συντονισμού: Ο όμιλος Nitro μπορεί να συμμετάσχει σε συντονισμό με το παρακείμενο άτομο άνθρακα, σταθεροποιώντας περαιτέρω τη δομή. Αυτή η απομάκρυνση συντονισμού απλώνει το αρνητικό φορτίο σε μια μεγαλύτερη περιοχή, μειώνοντας τη συγκέντρωσή του και καθιστώντας το μόριο πιο σταθερό.
* Επαγωγική επίδραση της ομάδας CH2CH2: Η ομάδα CH2CH2 είναι μια ομάδα-δοντάνιο ηλεκτρονίων. Στο `CH2CH2O -`, αυτή η ομάδα ωθεί την πυκνότητα ηλεκτρονίων προς το αρνητικά φορτισμένο άτομο οξυγόνου, αυξάνοντας περαιτέρω το αρνητικό φορτίο και καθιστώντας το μόριο λιγότερο σταθερό.
Συνοπτικά: Η παρουσία του ομίλου Nitro με ηλεκτρονίων-μειρό σε `O2NCH2CH2O -` και η ικανότητά της να συμμετέχει σε συντονισμό συμβάλλει σημαντικά στη μεγαλύτερη σταθερότητά του σε σύγκριση με το` CH2CH2O-'.