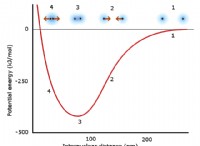
Ποιος τύπος δεσμού είναι πιθανό μεταξύ των ατόμων που είναι πολύ μακριά στον περιοδικό πίνακα;
* Διαφορά ηλεκτροαρνητικότητας: Τα άτομα μακριά από τον περιοδικό πίνακα έχουν σημαντική διαφορά στην ηλεκτροαρνητικότητα. Η ηλεκτροαρνητικότητα είναι η τάση ενός ατόμου να προσελκύει ηλεκτρόνια σε χημικό δεσμό.
* Μεταφορά ηλεκτρονίων: Το άτομο με υψηλότερη ηλεκτροαρνητικότητα θα προσελκύσει έντονα ηλεκτρόνια, λαμβάνοντας ουσιαστικά ένα ηλεκτρόνιο από το άτομο με χαμηλότερη ηλεκτροαρνητικότητα. Αυτό έχει ως αποτέλεσμα το σχηματισμό ιόντων:ένα θετικά φορτισμένο ιόν (κατιόν) και ένα αρνητικά φορτισμένο ιόν (ανιόν).
* Ηλεκτροστατική έλξη: Τα αντίθετα φορτισμένα ιόντα στη συνέχεια συγκρατούνται από μια ισχυρή ηλεκτροστατική έλξη, σχηματίζοντας έναν ιοντικό δεσμό.
Παράδειγμα: Το νάτριο (Na) και το χλώριο (CL) είναι πολύ μακριά στον περιοδικό πίνακα. Το νάτριο χάνει εύκολα ένα ηλεκτρόνιο για να γίνει ένα θετικό ιόν (Na+), ενώ το χλώριο κερδίζει ένα ηλεκτρόνιο για να γίνει αρνητικό ιόν (Cl-). Η προκύπτουσα ηλεκτροστατική έλξη σχηματίζει το χλωριούχο νάτριο ιοντικής ένωσης (NaCl) ή το αλάτι επιτραπέζιου.