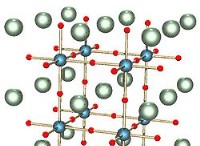
Ποιος είναι ο αριθμός συντονισμού ενός ιόντος τι κατιόν (α) δομή Na CL και (β) CS εξηγεί τον λόγο για αυτή τη διαφορά;
Αριθμός συντονισμού
Ο αριθμός συντονισμού ενός ιόντος αναφέρεται στον αριθμό των αντιθέτων ιόντων που το περιβάλλουν άμεσα σε ένα κρυσταλλικό πλέγμα.
(a) Δομή NaCl (δομή αλάτι βράχου)
* Αριθμός συντονισμού: Τόσο τα ιόντα Na⁺ όσο και CL⁻ έχουν έναν αριθμό συντονισμού 6 .
* Λόγος: Η δομή NaCl είναι ένα πλέγμα κυβικής (FCC) με επίκεντρο το πρόσωπο. Φανταστείτε έναν κύβο με ιόντα Na⁺ σε κάθε γωνιά και ιόντα CL⁻ στο κέντρο κάθε προσώπου.
* Κάθε ιόν Na⁺ περιβάλλεται από 6 ιόντα CL, και αντίστροφα.
* Αυτή η διάταξη σχηματίζει μια σφιχτά συσκευασμένη δομή, μεγιστοποιώντας την ηλεκτροστατική έλξη μεταξύ αντίθετα φορτισμένων ιόντων.
(b) Δομή CSCL (δομή χλωριούχου καισίου)
* Αριθμός συντονισμού: Τόσο τα ιόντα CS⁺ όσο και CL⁻ έχουν έναν αριθμό συντονισμού 8 .
* Λόγος: Η δομή CSCL είναι ένα απλό κυβικό πλέγμα. Φανταστείτε έναν κύβο με ιόν CS⁺ στο κέντρο και ιόντα CL⁻ σε κάθε γωνία ή αντίστροφα.
* Κάθε ιόν CS⁺ περιβάλλεται από 8 ιόντα CL, και αντίστροφα.
* Αυτή η δομή είναι λιγότερο σφιχτά συσκευασμένη από το NaCl. Το μεγαλύτερο μέγεθος του CS⁺ σε σύγκριση με το NA⁺ επιτρέπει περισσότερο χώρο γύρω από αυτό, επιτρέποντας έναν υψηλότερο αριθμό συντονισμού.
Βασική διαφορά
Η διαφορά στον αριθμό συντονισμού μεταξύ των δομών NaCl και CSCL οφείλεται κυρίως στη διαφορά μεγέθους Μεταξύ των κατιόντων (Na⁺ vs. CS⁺).
* μικρότερο κατιόν (na⁺): Το μικρότερο μέγεθος του Na⁺ επιτρέπει μια πιο σφιχτά συσκευασμένη δομή όπου περιβάλλεται μόνο από 6 ιόντα CL⁻.
* μεγαλύτερο κατιόν (CS⁺): Το μεγαλύτερο μέγεθος του CS⁺ δημιουργεί περισσότερο χώρο γύρω από αυτό, επιτρέποντάς του να φιλοξενήσει 8 ιόντα CL στη σφαίρα συντονισμού του.