Τι καθορίζεται από τις καιρικές συνθήκες ή όχι τα ηλεκτρόνια μεταφέρονται μεταξύ δύο ατόμων;
Εδώ είναι μια κατανομή:
* Ηλεκτροργατιστικότητα: Αυτό είναι ένα μέτρο της ικανότητας ενός ατόμου να προσελκύει ηλεκτρόνια σε χημικό δεσμό. Τα άτομα με υψηλότερη ηλεκτροαρνητικότητα έχουν ισχυρότερη έλξη στα ηλεκτρόνια.
* Κοινή χρήση εναντίον μεταφοράς:
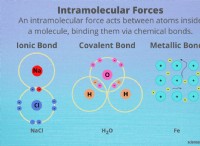
* ομοιοπολικοί δεσμοί: Όταν η διαφορά ηλεκτροαρνητικότητας μεταξύ δύο ατόμων είναι μικρά (συνήθως λιγότερο από 1,7 στην κλίμακα Pauling), τα άτομα μοιράζονται ηλεκτρόνια για να σχηματίσουν ένα σταθερό δεσμό. Αυτή η κατανομή μπορεί να είναι ίση (μη πολική ομοιοπολική) ή άνιση (πολική ομοιοπολική), ανάλογα με τη διαφορά ηλεκτροαρνητικότητας.
* Ιονικά ομόλογα: Όταν η διαφορά ηλεκτροαρνητικότητας μεταξύ δύο ατόμων είναι μεγάλη (συνήθως μεγαλύτερη από 1,7), το άτομο με υψηλότερη ηλεκτροαρνητικότητα παίρνει πλήρως τα ηλεκτρόνια από το άλλο άτομο. Αυτό δημιουργεί ιόντα (φορτισμένα σωματίδια) και οδηγεί σε ιοντικό δεσμό.
Συνοπτικά:
* Μικρή διαφορά ηλεκτροαρνητικότητας: Κοινή χρήση ηλεκτρονίων (ομοιοπολικός δεσμός)
* Μεγάλη διαφορά ηλεκτροαρνητικότητας: Μεταφορά ηλεκτρονίων (ιοντικός δεσμός)
Επιτρέψτε μου να ξέρω αν θέλετε να μάθετε περισσότερα σχετικά με την ηλεκτροαρνητικότητα ή τους διαφορετικούς τύπους χημικών δεσμών!