Τι διακρίνει ένα ισότοπο από ένα κανονικό στοιχείο;
Στοιχεία:
* Θεμελιώδη δομικά στοιχεία της ύλης: Τα στοιχεία είναι οι απλούστερες ουσίες που δεν μπορούν να κατανεμηθούν περαιτέρω με χημικά μέσα.
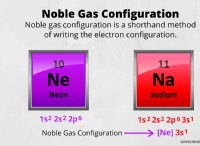
* ορίζεται από τον ατομικό αριθμό: The defining characteristic of an element is its atomic number , που αντιπροσωπεύει τον αριθμό των πρωτονίων στον πυρήνα του. Όλα τα άτομα ενός δεδομένου στοιχείου έχουν τον ίδιο αριθμό πρωτονίων.
* Παραδείγματα: Υδρογόνο (Η), άνθρακα (c), οξυγόνο (o)
ισότοπα:
* Παραλλαγές του ίδιου στοιχείου: Τα ισότοπα είναι άτομα του ίδιου στοιχείου (ο ίδιος ατομικός αριθμός) που διαφέρουν στον αριθμό των νετρονίων στον πυρήνα τους.
* ίδια χημική συμπεριφορά: Τα ισότοπα του ίδιου στοιχείου έχουν τον ίδιο αριθμό πρωτονίων και ηλεκτρονίων, έτσι γενικά συμπεριφέρονται με τον ίδιο τρόπο χημικά.
* Διαφορετική μάζα: Η διαφορά στον αριθμό των νετρονίων οδηγεί σε διαφορετικές ατομικές μάζες για ισότοπα.
* Παραδείγματα: Carbon-12 (6 πρωτόνια, 6 νετρόνια), άνθρακα-14 (6 πρωτόνια, 8 νετρόνια)
Συνοπτικά:
* Τα στοιχεία ορίζονται από τον αριθμό των πρωτονίων τους.
* Τα ισότοπα είναι παραλλαγές ενός στοιχείου με διαφορετικούς αριθμούς νετρονίων.
Σκεφτείτε το έτσι:Έχετε ένα σύνολο πανομοιότυπων δίδυμων. Και οι δύο έχουν το ίδιο DNA (ο ίδιος αριθμός πρωτονίων, ορίζοντάς τα με το ίδιο στοιχείο), αλλά ένα δίδυμο μπορεί να είναι ελαφρώς ψηλότερο ή βαρύτερο (διαφορετικός αριθμός νετρονίων, καθιστώντας τα ισότοπα).