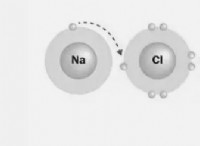
Τι είναι τα άτομα που δεσμεύονται σε ζεύγη;
Εδώ είναι μια κατανομή:
* Atom: Η βασική μονάδα ενός χημικού στοιχείου.
* Diatomic: Που σημαίνει "δύο άτομα".
* μόριο: Μια ομάδα δύο ή περισσότερων ατόμων που συγκρατούνται από χημικούς δεσμούς.
Παραδείγματα κοινών διατομικών μορίων:
* υδρογόνο (h₂): Το πιο άφθονο στοιχείο στο σύμπαν, υπάρχει φυσικά καθώς δύο άτομα υδρογόνου συνδέονται μαζί.
* οξυγόνο (o₂): Βασικό για τη ζωή στη γη, αναπνέουμε μόρια οξυγόνου.
* αζώτου (n₂): Αποτελεί την πλειοψηφία της ατμόσφαιρας μας.
* Φθορίνη (F₂): Ένα εξαιρετικά αντιδραστικό στοιχείο αλογόνου.
* Χλώριο (CL₂): Ένα πράσινο-κίτρινο αέριο που χρησιμοποιείται συνήθως σε απολυμαντικά.
* Βρωμίνη (BR₂): Ένα κοκκινωπό-καφέ υγρό που εξατμίζεται εύκολα.
* ιώδιο (i₂): Ένα μοβ στερεό που χρησιμοποιείται σε αντισηπτικά διαλύματα.
Είναι σημαντικό να θυμόμαστε ότι δεν σχηματίζουν όλα τα διατομικά μόρια. Ορισμένα στοιχεία, όπως το ήλιο (He) και το νέον (NE), υπάρχουν ως μεμονωμένα άτομα και άλλα σχηματίζουν πιο σύνθετα μόρια με πολλαπλά άτομα.