Τι σημαίνει και τι σημαίνει το pH;
Το pH σημαίνει δυναμικό υδρογόνο με το "p" να σημαίνει δυναμικό και το "H" να σημαίνει υδρογόνο. Η κλίμακα pH είναι μια κλίμακα που χρησιμοποιείται για την ταξινόμηση της σχετικής βασικότητας ή οξύτητας των ουσιών σε σχέση με άλλες ουσίες, με βάση την ποσότητα της δραστηριότητας ιόντων υδρογόνου σε μια ουσία.
Η κλίμακα είναι λογαριθμικής φύσης, που σημαίνει ότι κάθε ακέραια τιμή pH αντιπροσωπεύει μια αλλαγή 10 φορές την προηγούμενη τιμή. Η κλίμακα pH βασίζεται γύρω στο pH 7, το οποίο είναι ουδέτερο και αντιπροσωπεύει ουσίες που δεν είναι ούτε οξύ ούτε βάση.
Η βάση για την κλίμακα pH
Ακόμα κι αν δεν είστε καλά εξοικειωμένοι με τις έννοιες των οξέων και των βάσεων, σίγουρα έχετε κάποια έκθεση σε αυτά. Οι βασικές ουσίες είναι πράγματα όπως η μαγειρική σόδα, ενώ οι όξινες ουσίες είναι πράγματα όπως ο χυμός πορτοκαλιού και η σόδα. Οι ουσίες ταξινομούνται ως βάση ή ως βάση οξέος με βάση τη συγκέντρωση ιόντων υδρογόνου που έχει η ουσία. Το Η σε pH αντιπροσωπεύει το επίπεδο δραστηριότητας ιόντων υδρογόνου σε ένα δεδομένο διάλυμα. Επομένως, μπορείτε να ορίσετε όξινα και βασικά διαλύματα ως εξής:
Ένα όξινο διάλυμα είναι ένα διάλυμα με επίπεδα ιόντων υδρογόνου μεγαλύτερα από την ποσότητα που βρίσκεται στο καθαρό νερό (που βρίσκεται στο ουδέτερο επτά). Ένα βασικό διάλυμα, αντίθετα, έχει συγκέντρωση ιόντων υδρογόνου χαμηλότερη από αυτή του νερού.

Δεδομένου ότι το καθαρό νερό λειτουργεί ως το ουδέτερο σημείο στην κλίμακα του pH, ας δούμε τις ιδιότητες του νερού και ας το τοποθετήσουμε στο πλαίσιο των ιόντων υδρογόνου. Ο ιονισμός του νερού αναφέρεται στο πώς ένα μικρό ποσοστό των μορίων του νερού σε μια δεδομένη ποσότητα νερού θα δημιουργήσει αυθόρμητα ιόντα υδρογόνου καθώς διασπώνται ή χωρίζονται σε μικρότερα σωματίδια. Αυτό μερικές φορές αναφέρεται ως αυτοιονισμός. Η διαδικασία του αυτοιονισμού παράγει ίσους αριθμούς ιόντων υδροξειδίου (ΟΗ-) και ιόντων υδρογόνου (Η+). Σημειώστε ότι τα ιόντα υδρογόνου συνήθως συνδέονται απευθείας με ένα κοντινό μόριο νερού για να σχηματίσουν υδρόνιο (H3O+). Αυτό σημαίνει ότι δεν υπάρχει στην πραγματικότητα μια δέσμη ιόντων υδρογόνου που επιπλέουν στο νερό. Ωστόσο, οι επιστήμονες εξακολουθούν να χρησιμοποιούν τον ιονισμό του νερού και των ιόντων υδρογόνου που παράγουν ως τρόπο για να δημιουργήσουν μια κλίμακα που επιτρέπει τη σύγκριση του υδρογόνου σε επίπεδα σε άλλα διαλύματα. Τα ιόντα υδροξειδίου συνήθως απλώς επιπλέουν μέσα στο διάλυμα, σε αντίθεση με τα ιόντα υδρογόνου.
Όσον αφορά τον αριθμό των ιόντων υδρογόνου που παράγονται μέσω του αυτοιονισμού, η ποσότητα είναι ίση με 1 x 10^-7 M (υποθέτοντας ότι είναι καθαρό νερό). Η σημείωση αναφέρεται σε μολύβια ανά λίτρο νερού. Ο αριθμός των μορίων ιονισμένου νερού είναι ένα απίστευτα μικρό ποσοστό του συνολικού αριθμού μορίων νερού που βρίσκονται σε οποιαδήποτε ποσότητα καθαρού νερού.
Διαλύματα οξέων και βασικές λύσεις
Τώρα που έχουμε δημιουργήσει ένα σημείο αναφοράς για τη βασικότητα και την οξύτητα των διαλυμάτων, μπορούμε να συζητήσουμε πώς ορίζονται τα οξέα και οι βάσεις. Όξινα διαλύματα είναι εκείνα τα διαλύματα που έχουν μεγαλύτερη συγκέντρωση Η+ από το καθαρό νερό, ενώ τα βασικά διαλύματα είναι εκείνα που έχουν συγκέντρωση Η+ μικρότερη από αυτή του καθαρού νερού. Για να το θέσω αλλιώς:
Βάση =συγκέντρωση Η+ <1 x 10^-7 M
Οξύ =συγκέντρωση Η+> 1 x 10^-7 M
Η συγκέντρωση των ιόντων υδρογόνου σε ένα διάλυμα δίνεται συνήθως σε όρους pH, το οποίο υπολογίζεται ως το αντίστροφο log της συγκέντρωσης ιόντων υδρογόνου για αυτό το δεδομένο διάλυμα.
pH =-log10[H+]
Έτσι, αν βάλετε τη συγκέντρωση ιόντων υδρογόνου του νερού σε αυτόν τον τύπο θα έχετε μια τιμή 7,0 ή το ουδέτερο pH στην κλίμακα pH. Όπως ίσως μπορείτε να μαντέψετε, ουσίες που παράγονται κυρίως από νερό, όπως το κυτοσόλιο που βρίσκεται στα κύτταρα ή το αίμα στο ανθρώπινο σώμα, έχουν τιμές pH πολύ κοντά στο ουδέτερο επτά. Οξέα και βάσεις μπορούν να προστεθούν σε ένα διάλυμα με βάση το νερό, μετατοπίζοντας τη συγκέντρωση αυτού του διαλύματος μακριά από το ουδέτερο σημείο pH. Οι βάσεις συνήθως αυξάνουν το επίπεδο του pH μέσω της εισαγωγής υδροξειδίου στο περιβάλλον, το οποίο συλλέγει τα ιόντα υδρογόνου και τα τραβάει έξω από το διάλυμα. Εν τω μεταξύ, όξινες ουσίες είναι εκείνες που αυξάνουν τη συγκέντρωση ιόντων υδρογόνου διασπώντας και εισάγοντας ένα από τα άτομα υδρογόνου του στο διάλυμα.
Όσο πιο ισχυρό είναι το οξύ, τόσο πιο γρήγορα θα αποικοδομηθεί και θα απελευθερώσει H+. Ένα παράδειγμα ισχυρού οξέος είναι το HCl, το οποίο όταν συνδυάζεται με νερό διασπάται γρήγορα και πλήρως σε ιόντα χλωρίου και υδρογόνου. Αντίθετα, τα αδύναμα οξέα όπως το ξύδι δεν διασπώνται εντελώς. Μια ισχυρή βασική ουσία απελευθερώνει ιόντα υδροξειδίου ικανά να απορροφούν Η+ όταν βρίσκεται στο νερό, αποικοδομώντας πλήρως όπως θα κάνει μια ουσία ισχυρού οξέος. Ένα παράδειγμα ισχυρής βάσης είναι το υδροξείδιο του νατρίου.
Κλίμακα αντοχής pH
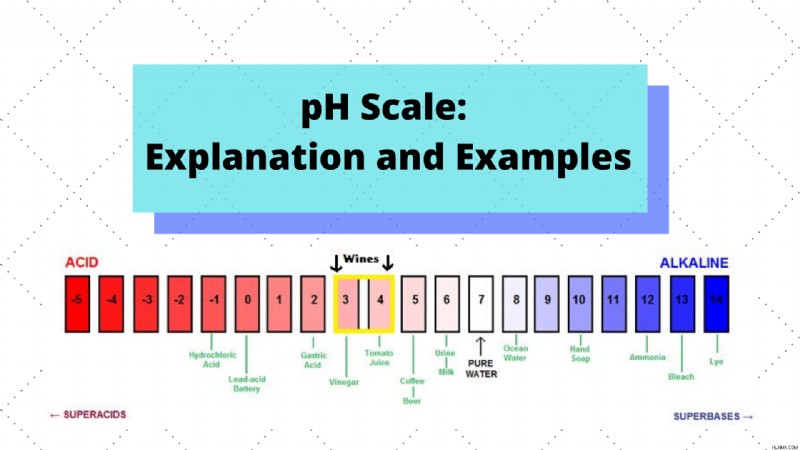
Όπως αναφέρθηκε προηγουμένως, η κλίμακα pH βοηθά στην ταξινόμηση διαφόρων χημικών συνθέσεων ως προς τη βασικότητά τους (ονομάζεται επίσης αλκαλικότητα) και την οξύτητά τους. Είναι λογαριθμική φύση σημαίνει ότι για κάθε αύξηση μιας μονάδας pH που συμβαίνει, υπάρχει μια δεκαπλάσια αύξηση στις συγκεντρώσεις του Η+. Ενώ υπάρχουν ορισμένες ουσίες που μπορούν να πέσουν έξω από το εύρος pH 0 έως 14, τα περισσότερα διαλύματα εμπίπτουν σε αυτό το εύρος και επομένως η κλίμακα pH συνήθως αντιπροσωπεύεται από 0 έως 14, με τις βασικές ουσίες να είναι οποιαδήποτε τιμή πάνω από επτά και τις όξινες ουσίες οποιαδήποτε τιμή κάτω από το ουδέτερο 7.
Ουσίες που βρίσκονται στα άκρα της κλίμακας του pH, είτε εξαιρετικά βασικές είτε εξαιρετικά όξινες ουσίες μπορεί να είναι αρκετά επιβλαβείς για το οργανικό υλικό, προκαλώντας σημαντική βλάβη στα κύτταρα. Τόσο οι πολύ βασικές όσο και οι πολύ όξινες ουσίες μπορεί να είναι διαβρωτικές στη φύση, καταστρέφοντας τον ιστό των ανθρώπων. Το pH του διαλύματος, καθώς και η ποσότητα του διαλύματος στο οποίο εκτίθεται κάποιος και πόσο καιρό εκτίθενται σε αυτό, είναι όλοι παράγοντες που καθορίζουν πόση ζημιά θα κάνει η ουσία. Ίσως έχετε παρατηρήσει ότι το γαστρικό οξύ, το οξύ του στομάχου σας, είναι μια πολύ όξινη ουσία. Πώς προστατεύεται το σώμα σας από αυτό το οξύ; Υπάρχουν ορισμένα κύτταρα του στομάχου που δημιουργούνται ειδικά για να λειτουργούν ως φράγμα μεταξύ του γαστρικού οξέος και των άλλων κυττάρων του σώματος, τα οποία δημιουργούνται και θυσιάζονται συνεχώς.
Παραδείγματα
Μερικά παραδείγματα κοινών διαλυμάτων και οι τιμές pH που διαθέτουν είναι:
- Γάλα – ελαφρώς όξινο με τιμή pH περίπου 6,5.
- Βροχή – ελαφρώς όξινη με τιμή pH περίπου 5,5.
- Καφές – ήπια όξινος με τιμή pH περίπου 4,8.
- Χυμός ντομάτας – ήπια όξινος με pH περίπου 3,0
- Οξύ μπαταρίας – εξαιρετικά όξινο με τιμή pH περίπου 1,0.
- Αίμα – ελαφρώς βασικό με ph περίπου 7,3
- Θαλασσινό νερό – ελαφρώς βασικό με pH περίπου 8,0.
- Μαγειρική σόδα – ελαφρώς βασική με pH περίπου 8,0.
- Γάλα μαγνησίας – μέτρια βασικό με pH περίπου 10,6
- Lye – Πολύ βασικό με pH περίπου 13,5




