Γεγονότα για το Βηρύλλιο 1
Το βηρύλλιο είναι το τέταρτο στοιχείο του περιοδικού πίνακα. Αυτά τα στοιχεία για το βηρύλλιο περιέχουν χημικά και φυσικά δεδομένα μαζί με γενικές πληροφορίες και ιστορικό.

Βασικά στοιχεία για το βηρύλλιο
Όνομα: Βηρύλλιο
Ατομικός αριθμός: 4
Σύμβολο στοιχείου: Be
Ομάδα: 2
Περίοδος: 2
Αποκλεισμός: s
Οικογένεια στοιχείων: Αλκαλική Γη
Ατομική μάζα: 9.012182(3)
Διαμόρφωση ηλεκτρονίου: [He]2s (συντομογραφία) ή 1s2s (πλήρης)
Ανακάλυψη: Louis-Nicholas Vauquelin το 1798.
Ο Vauquelin διερεύνησε τις χημικές ιδιότητες των βερύλων. Τα βηρύλια διατίθενται σε μεγάλη ποικιλία χρωμάτων, αλλά φαίνεται να έχουν παρόμοια χημικά χαρακτηριστικά. Απομόνωσε μια ένωση που περιείχε ένα άγνωστο στοιχείο με γλυκιά γεύση. Το καθαρό βηρύλλιο απομονώθηκε για πρώτη φορά το 1828 από τον Γερμανό χημικό Friederich Wöhler και τον Γάλλο χημικό Antoine Bussy ανεξάρτητα ο ένας από τον άλλο.
Προέλευση ονόματος: Ο Vauquelin ονόμασε το στοιχείο του από την ουσία που ερευνούσε, beryl. Πρώτα ονόμασε την ουσία Γη του βηρυλίου, αλλά άλλαξε σε γλυκένιο για να αντανακλά τη γλυκιά γεύση. Ο Wöhler πρότεινε να αλλάξει το όνομα από τη γευστική ιδιότητα αφού υπάρχουν πολλά στοιχεία με γλυκιά γεύση. Ονόμασε το στοιχείο βηρύλλιο από την ελληνική λέξη βηρύλλος για βηρύλ.
Φυσικά ισότοπα:
Το βηρύλλιο είναι σχεδόν 100% βηρύλλιο-9. Δύο άλλα ισότοπα μπορούν να βρεθούν σε ίχνη.
Είναι
Το βηρύλλιο-7 είναι ένα ραδιενεργό ισότοπο που περιέχει 3 νετρόνια. Διασπάται σε Li μέσω της σύλληψης ηλεκτρονίων. Ο χρόνος ημιζωής του είναι 53,12 ημέρες.
Είναι
Το βηρύλλιο-9 είναι το πιο κοινό φυσικό ισότοπο. Περιέχει 5 νετρόνια και είναι σταθερό.
Είναι
Το βηρύλλιο-10 είναι ένα ραδιενεργό ισότοπο που περιέχει 6 νετρόνια. Διασπάται σε Β με β- διάσπαση με χρόνο ημιζωής 1,36 εκατομμύρια χρόνια.

Φυσικά δεδομένα
Πυκνότητα: 1,85 g/cm
Σημείο τήξης: 1560 K (1287 ºC ή 2349 ºF)
Σημείο βρασμού: 3243 K (2970 ºC ή 5338 ºF)
Κατάσταση στους 20ºC: Στερεά
Heat of Fusion: 12,2 kJ/mol
Θερμότητα εξάτμισης: 292 kJ/mol
Μοριακή θερμική χωρητικότητα: 16.443 J/mol·K
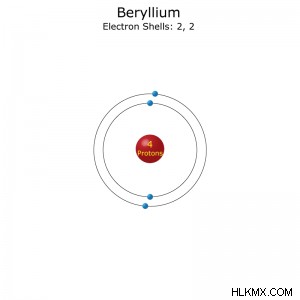
Ατομικά δεδομένα
Ατομική ακτίνα: 1.12 Å (εμπειρικό)
Ομοιοπολική ακτίνα: 0,96 Å
Ακτίνα Van der Waals: 1,82 Å
Συγγένεια ηλεκτρονίων: μη σταθερό
Ηλεκτραρνητικότητα: (Κλίμακα Pauling):1,85
1 Ενέργεια Ιονισμού: 899,504 kJ/mol
2 Ενέργεια Ιονισμού: 1757,108 kJ/mol
3 Ενέργεια Ιονισμού: 14848,767 kJ/mol
4 Ενέργεια Ιονισμού: 21006.658 kJ/mol
Συνήθεις καταστάσεις οξείδωσης: +2 (κοινό), +1 (ασυνήθιστο)

Διασκεδαστικά γεγονότα για το Βηρύλλιο
- Το βηρύλλιο είναι ένα μαλακό, ασημί-λευκό μέταλλο με χαμηλή πυκνότητα. Οι κρύσταλλοι είναι δυνατοί αλλά εύθραυστοι.
- Το βηρύλλιο προστίθεται σε κράματα για την αύξηση της ηλεκτρικής και θερμικής αγωγιμότητας.
- Τα εργαλεία βηρυλλίου είναι κατασκευασμένα για να αποτρέπουν τη δημιουργία σπινθήρων όταν το εργαλείο χτυπά άλλο μέταλλο. Αυτά τα εργαλεία είναι ζωτικής σημασίας σε περιβάλλοντα όπου ο κίνδυνος φλόγας ή εκρήξεων είναι υψηλός.
- Το βηρύλλιο έχει το υψηλότερο σημείο τήξης από τα ελαφρά μέταλλα.
- Βηρύλλιο ανακαλύφθηκε κατά τη διερεύνηση των βηρύλων. Τα βηρύλια είναι ορυκτά με χημικό τύπο Be3 Al2 (SiO3 )6 που κυκλοφορούν σε πολλά διαφορετικά χρώματα.
- Βρέθηκε ότι το βηρύλλιο έχει γλυκιά γεύση. Ένα τυπικό τεστ για τους πρώτους χημικούς ήταν το τεστ γεύσης. Τι γεύση έχει το δείγμα; Σήμερα, γνωρίζουμε ότι το βηρύλλιο και οι ενώσεις του είναι όλα εξαιρετικά τοξικά και καρκινογόνα.
- Ένα πρώιμο όνομα για το βηρύλλιο ήταν glyceynum μετά την ελληνική λέξη glykis που σημαίνει γλυκό.
- Το βηρύλλιο είναι σχετικά διαφανές στις ακτινογραφίες. Το φύλλο βηρυλλίου χρησιμοποιείται ως παράθυρο για εκπομπούς ακτίνων Χ.
- Το βηρύλλιο χρησιμοποιείται στα πυρηνικά ως συντονιστές και ανακλαστήρες νετρονίων.
- Το βηρύλλιο χρησιμοποιείται ως στόχος για την παραγωγή νετρονίων. Όταν βομβαρδίζεται με σωματίδια άλφα (πυρήνες ηλίου), η προκύπτουσα αντίδραση μπορεί να παράγει υψηλή απόδοση νετρονίων.
Μάθετε περισσότερα σχετικά με τα στοιχεία στον περιοδικό πίνακα.