Τι είναι το φθόριο; Φθόριο vs Φθόριο
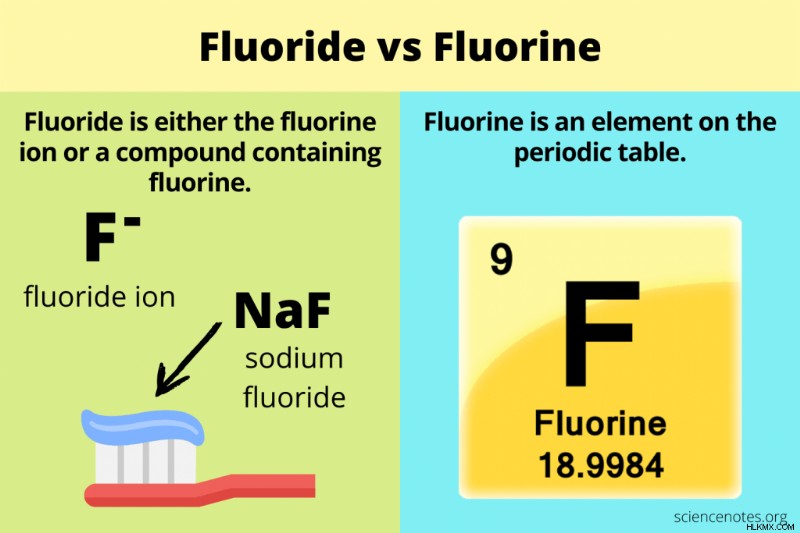
Υπάρχει σύγχυση σχετικά με τη διαφορά μεταξύ φθορίου και φθορίου. Το φθόριο σχετίζεται με το φθόριο, αλλά οι δύο χημικές ουσίες δεν είναι ίδιες. Φθόριο είναι χημικό στοιχείο, ενώ το φθόριο είναι είτε το ιόν αυτού του στοιχείου είτε μια ένωση που το περιέχει. Το σύμβολο F σημαίνει φθόριο, ενώ το φθόριο είναι F ή αλλιώς περιέχεται σε μια ένωση (π.χ. NaF).
Το καθαρό φθόριο είναι ένα ανοιχτό κίτρινο αέριο που εμφανίζεται στον φλοιό της Γης και διαλύεται στο θαλασσινό νερό. Όμως, το φθόριο είναι ένα αντιδραστικό στοιχείο, επομένως σπάνια εμφανίζεται σε καθαρή μορφή. Σχηματίζει το ιόν F και συνδυάζεται με άλλα στοιχεία, σχηματίζοντας ενώσεις και μέταλλα.
Παραδείγματα φθορίου
Τα παραδείγματα φθορίου περιλαμβάνουν το ιόν και τις ενώσεις που περιέχουν φθόριο ως ανιόν:
- Ιόν φθορίου – F
- Εξαφθοριούχο θείο – SF6
- Φθοριούχο ασβέστιο – CaF2
- Φθοριούχο νάτριο – NaF
- φθοροπυριτικό νάτριο – Na2 SiF6
Χρήσεις φθορίου
Η πιο γνωστή χρήση του φθορίου είναι στην πρόληψη της κοιλότητας, αλλά έχει άλλες εφαρμογές.
- Πρόληψη κοιλότητας (φθοριούχο νάτριο, μονοφθοροφωσφορικό νάτριο)
- Θεραπεία οστεοπόρωσης
- Τύξη αλουμινίου (κρυόλιθος, Na3 AlF3 )
- Κατασκευή χάλυβα (φθορίτης, CaF2 )
- Παραγωγή φθοράνθρακα (υδροφθόριο, HF)
- Βιοχημικές αναλύσεις
- Μπαταρίες ιόντων φθορίου
Επιπτώσεις και κίνδυνοι από φθόριο και φθόριο στην υγεία
Το στοιχειακό φθόριο είναι εξαιρετικά τοξικό για τον άνθρωπο και άλλους ζωντανούς οργανισμούς. Τα αποτελέσματά του είναι συγκρίσιμα με εκείνα του καθαρού χλωρίου, ερεθίζοντας τα μάτια και τους βλεννογόνους και βλάπτουν το συκώτι και τα νεφρά. Ορισμένα φθόριο είναι επίσης εξαιρετικά επικίνδυνα, όπως το υδροφθόριο, το οποίο είναι πιο γνωστό ως υδροφθορικό οξύ.
Όμως, σε μικρές ποσότητες, το φθόριο είναι πιθανότατα ένα μικροθρεπτικό συστατικό. Η ημερήσια συνιστώμενη ποσότητα εξαρτάται κυρίως από την ηλικία και κυμαίνεται από 0,6 mg/ημέρα έως 4,0 mg/ημέρα. Η ανεπάρκεια φθορίου αυξάνει τον κίνδυνο εμφάνισης τερηδόνας. Η τοπική εφαρμογή μιας φθοριούχου ένωσης, όπως το φθοριούχο νάτριο, βοηθά στην πρόληψη της τερηδόνας ενώ έχει ως αποτέλεσμα την ελάχιστη πρόσληψη φθορίου. Η κατάποση υπερβολικής ποσότητας φθορίου οδηγεί σε οδοντική φθορίωση, μια κατάσταση που κυμαίνεται από αβλαβή λευκά σημάδια στα δόντια έως καφέ, εξασθενημένα δόντια. Η υπερβολική κατάποση φθορίου οδηγεί επίσης σε έλκη στομάχου και σκελετική φθορίωση, η οποία είναι μια χρόνια ασθένεια των οστών και των αρθρώσεων. Αν και είναι ευεργετικό σε μικρές δόσεις, το φθόριο γίνεται θανατηφόρο σε επίπεδα μεταξύ 32 και 64 mg/kg σωματικού βάρους. Το ασφαλές ανώτατο όριο κατανάλωσης φθορίου είναι 7 mg/ημέρα (Ευρωπαϊκή Ένωση) ή 10 mg/ημέρα (Ηνωμένες Πολιτείες) για ενήλικες ή 0,10 mg/kg ημερησίως για βρέφη και παιδιά έως 8 ετών.
Διαιτητικές πηγές φθορίου και φθορίου
Υπάρχουν πολλές κοινές πηγές φθορίου και φθορίου στη διατροφή:
- Φθοριούχο νερό
- Μαύρο τσάι
- Σταφίδες
- Κρασί
- Πατάτες
- Αρνί
- Αβοκάντο
- Σπανάκι
- Ροδάκινα
- Μαρούλι
- Ραπανάκια
Από αυτές τις πηγές, το τσάι περιέχει τα υψηλότερα επίπεδα φθορίου. Ένα φλιτζάνι μαύρο τσάι παρέχει περίπου 0,884 χιλιοστόγραμμα φθορίου.
Αναφορές
- Aigueperse, Jean; Mollard, Paul; Devilliers, Didier; Chemla, Marius; Faron, Robert; Romano, René; Cuer, Jean Pierre (2000). «Ενώσεις Φθορίου, Ανόργανες». Ullmann's Encyclopedia of Industrial Chemistry . ISBN 978-3527306732. doi:10.1002/14356007.a11_307
- IPCS (2002). Περιβαλλοντικά κριτήρια υγείας 227 (Φθόριο) . Γενεύη:Διεθνές Πρόγραμμα για τη Χημική Ασφάλεια, Παγκόσμιος Οργανισμός Υγείας. ISBN 978-92-4-157227-9.
- Malinowska, E.; Inkielewicz, Ι.; Czarnowski, W.; Szefer, P. (2008). «Αξιολόγηση της συγκέντρωσης φθορίου και της ημερήσιας πρόσληψης από τον άνθρωπο από αφεψήματα τσαγιού και βοτάνων». Food Chem. Toxicol . 46 (3):1055–61. doi:10.1016/j.fct.2007.10.039
- Yeung, C.A. (2008). «Μια συστηματική ανασκόπηση της αποτελεσματικότητας και της ασφάλειας της φθορίωσης». Οδοντιατρική βάσει τεκμηρίων . 9 (2):39–43. doi:10.1038/sj.ebd.6400578




