Ορισμός μονοπρωτικού οξέος και παραδείγματα
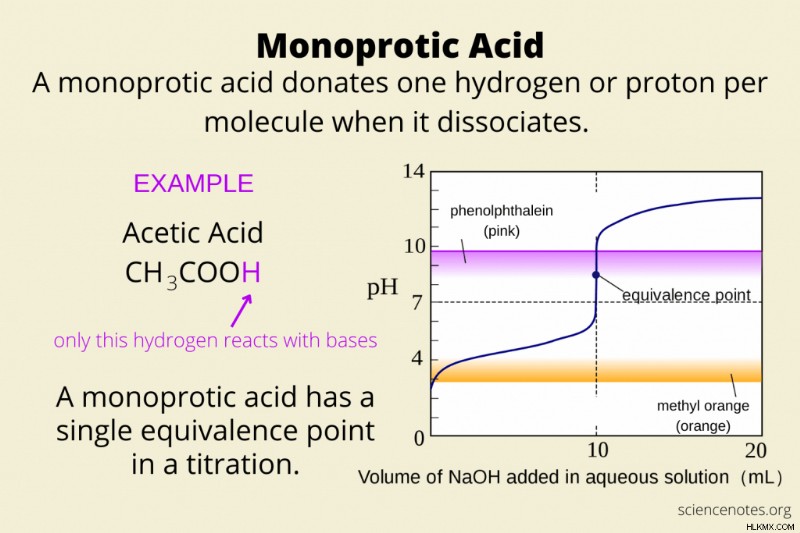
Στη χημεία, ένα μονοπρωτικό οξύ είναι ένα οξύ που δίνει ένα ιόν υδρογόνου (Η) ή πρωτόνιο ανά μόριο όταν διασπάται στο νερό. Ένα άλλο όνομα για ένα μονοπρωτικό οξύ είναι μονοβασικό οξύ . Ένα μονοπρωτικό οξύ (ΗΑ) διασπάται σύμφωνα με την ακόλουθη διαδικασία:
HA (aq) + H2 O (l) ⇌ H3 O (aq) + A (aq)
Παραδείγματα μονοπρωτικών οξέων
Τα μονοπρωτικά οξέα περιλαμβάνουν τόσο ισχυρά όσο και αδύναμα οξέα. Τα οξέα που περιέχουν ένα μόνο άτομο υδρογόνου (Η) είναι προφανές παράδειγμα, αλλά ορισμένα οξέα με πολλαπλά άτομα υδρογόνου είναι επίσης κατάλληλα. Για παράδειγμα, οργανικά οξέα που περιέχουν μία ομάδα καρβοξυλικού οξέος (R−COOH ή R−CO2 Η) είναι μονοπρωτικά.
Ακολουθούν παραδείγματα μονοπρωτικών οξέων:
- Οξικό οξύ (CH3 COOH)
- Βενζοϊκό οξύ (C6 H5 COOH)
- Μυρμηκικό οξύ (HCOOH)
- Υδροβρωμικό οξύ (HBr)
- Υδροχλωρικό οξύ (HCl)
- Υδροφθορικό οξύ (HF)
- Υδροϊωδικό οξύ (HI)
- Νιτρικό οξύ (HNO3 )
Παραδείγματα πολυπρωτικών οξέων
Τα πολυπρωτικά οξέα δίνουν περισσότερα από ένα υδρογόνο ή πρωτόνια όταν διασπώνται. Ένα διπρωτικό οξύ δωρίζει δύο πρωτόνια, ενώ ένα τριπρωτικό οξύ δωρίζει τρία πρωτόνια. Η επακόλουθη απώλεια κάθε πρωτονίου γίνεται πιο δυσμενής, αλλά όλες οι συζευγμένες βάσεις ενός πολυπρωτικού οξέος υπάρχουν σε υδατικό διάλυμα.
Διπρωτικά οξέα
Αναζητήστε το H2 εντός του τύπου ενός διπρωτικού οξέος:
- Θειικό οξύ:H2 SO4
- Ανθρακικό οξύ:H2 CO3
- Οξαλικό οξύ:C2 H2 O4
Τριπρωτικά οξέα
- Φωσφορικό οξύ:H3 PO4
- Αρσενικό οξύ:H3 AsO4
- Κιτρικό οξύ:C6 H8 O7
Πώς να αναγνωρίζετε τα μονοπρωτικά οξέα
Δύο τρόποι αναγνώρισης μονοπρωτικών οξέων είναι οι χημικοί τύποι και οι καμπύλες τιτλοδότησης τους.
Ένα μονοπρωτικό οξύ περιέχει είτε ένα μόνο άτομο υδρογόνου (π.χ. HCl) είτε μια μοναδική ομάδα καρβοξυλικού οξέος (π.χ., CH3 COOH).
Το γράφημα μιας τιτλοδότησης μονοπρωτικού οξέος δείχνει ένα μόνο σημείο ισοδυναμίας. Αντίθετα, ένα διπρωτικό οξύ έχει δύο σημεία ισοδυναμίας και ένα τριπρωτικό οξύ έχει τρία σημεία ισοδυναμίας.
Αναφορές
- Ebbing, Darrell; Gammon, Steven D. (1 Ιανουαρίου 2016). Γενική Χημεία . Cengage Learning. ISBN 9781305887299.
- Petrucci R.H., Harwood, R.S.; Ρέγγα, F.G. (2002). Γενική Χημεία (8η έκδ.). Prentice-Hall. ISBN 0-13-014329-4.
- Skoog, D.A; West, D.M.; Holler, J.F.; Crouch, S.R. (2004). Βασικές αρχές της αναλυτικής χημείας (8η έκδ.). Τόμσον Μπρουκς/Κόουλ. ISBN 0-03-035523-0.
- Zumdahl, Steven S. (1997). Χημεία (4η έκδ.). Βοστώνη:Houghton Mifflin. ISBN 9780669417944.