Enol
Η ενόλη είναι ένα οργανικό μόριο που έχει μια ομάδα υδροξυλίου συνδεδεμένη με ένα διπλό άτομο άνθρακα και επομένως συνήθως ορίζεται με την ομαδοποίηση C=C. (OH). Τα αλκένια που έχουν μια ομάδα υδροξυλίου συνδεδεμένη με μερικά από τα μόρια άνθρακα των διπλών δεσμών αναφέρονται ως ενόλες. Τα αλκένια με ομάδες υδροξυλίου σε κάθε πλευρά του διπλού δεσμού είναι γνωστά ως αρχικά. Τα ενολικά είναι τα αποπρωτονισμένα ανιόντα των ενολών. Η ρεδουκτόνη είναι ένα μόριο με σύνθεση ενδιόλης καθώς και μια καρβονυλική ομάδα συνδεδεμένη με αυτήν επίσης. Σύμφωνα με τον διπλό δεσμό C=C με κάτι σαν το κοντινό αλκοόλ, οι ενόλες και οι ενδιόλες παρουσιάζουν χημικά χαρακτηριστικά που προκαλούν ταυτομερισμό κετο-ενόλης.
Διαφορά μεταξύ Enolate και Enol
Οι ενόλες, οι ενολικές ενώσεις και οι εναμίνες είναι τρία είδη οργανικών ενώσεων. Οι ενόλες είναι μερικές φορές γνωστές ως αλκενόλες. Είναι επειδή η ενόλη παράγεται με συνδυασμό της ομάδας αλκενίου συμπεριλαμβανομένης μιας ομάδας αλκοόλης. Οι ενόλες παίρνουν πτητική μορφή αφού είναι ενδιάμεσα μόρια κατά τις χημικές αντιδράσεις. Οι ενόλες είναι τα δομικά στοιχεία των ενολών. Η συζευγμένη βάση μιας ενόλης ονομάζεται ενολικό. Κάθε φορά που λαμβάνεται ένα ιόν υδρογόνου από την ομάδα υδροξυλίου μιας ενόλης, σχηματίζεται το ενολικό. Οι εναμίνες περιλαμβάνουν ενώσεις αμίνης που περιέχουν διπλό δεσμό μεταξύ της ομάδας αμίνης και του ατόμου άνθρακα. Η χημική αντιδραστικότητα των ενολικών σε εναμίνες είναι σχεδόν συγκρίσιμη. Οι ενόλες λαμβάνουν μια ομάδα υδροξυλίου δίπλα σε έναν διπλό δεσμό C=C, ενώ οι ενολικές έχουν αρνητικό φορτίο σε αυτό το άτομο οξυγόνου μιας ενόλης και οι εναμίνες λαμβάνουν μια ομάδα αμίνης δίπλα σε έναν διπλό δεσμό C=C.
Σύνθεση ενολικών και ενολών
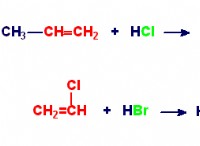
Οι ενόλες φαίνεται να είναι αρωματικοί υδρογονάνθρακες και ισομερή κετόνης με απλό άλφα υδρογόνο που έχει απορριφθεί και αντικαθίσταται σε αυτό το άτομο οξυγόνου της καρβονυλικής ομάδας. Δεδομένου ότι έχει μια ομάδα C=C καθώς και μια -ΟΗ, αυτό το μόριο ονομάζεται εν/όλη ή ενόλη. Για την παρασκευή ενολών χρησιμοποιούνται αποκλειστικά καρβονυλικά στοιχεία που περιέχουν άλφα υδρογόνα. Μπορούν να γίνουν με κατάλυση οξέος και βάσης και επομένως είναι εξαιρετικά αντιδραστικά με ηλεκτρόφιλα όπως το βρώμιο μόλις δημιουργηθούν. Η δημιουργία των ενολών αναφέρεται ως «ενολίωση». Απαιτείται κατάλυση με οξύ ή ίσως βάση.
Ταυτομερισμός κετο-ενόλης
Στην οργανική χημεία, ο ταυτομερισμός της κετο-ενόλης είναι πράγματι μια χημική ισορροπία μεταξύ μιας κετομορφής και επίσης μιας ενόλης (αλκοόλης). Εδώ, μεταξύ των εκδόσεων keto και enol, λέγεται ότι εμφανίζονται ταυτομερή. Αυτός ο ισομερισμός είναι γνωστός ως ταυτομερισμός επειδή η αντίδραση 2 τύπων απαιτεί την κίνηση ενός τέτοιου ιόντος άλφα υδρογόνου και την αναδιάταξη ενός ζεύγους ηλεκτρονίων. Τα ταυτομερή φαίνεται να είναι ισομερή που ποικίλλουν μόνο στον τρόπο με τον οποίο μετακινούν ένα άτομο υδρογόνου από το ένα άτομο στο άλλο. Μεταξύ των ενολών και των αντίστοιχων κετο ισομερών προκύπτουν ταυτομερή. Το ταυτομερές κετο είναι συχνά ουσιαστικά πιο στιβαρό από αυτό της μορφής ενόλης, με K's περίπου 10 έως -5ης ισχύος.
Ενολισμός καταλυόμενης βάσης
Η ενολίωση μπορεί να λάβει χώρα είτε υπό βασικές είτε όξινες συνθήκες, αν και η καταλυόμενη με βάση ενολίωση φαίνεται να είναι η πιο διαδεδομένη μέθοδος. Είναι καλή ιδέα να ελέγξετε αρχικά την ενολίωση κάτω από τις βασικές ρυθμίσεις.
Μια κετόνη ή ίσως μια αλδεΰδη συμπεριφέρεται ως οξύ Bronsted υπό βασικές συνθήκες, δίνοντας ένα πρωτόνιο από έναν α-άνθρακα σε μια βάση μέσα στο διάλυμα. Το ενολικό ανιόν σταθεροποιείται συντονισμένα ως αποτέλεσμα αυτής της διαδικασίας. Επειδή το καρβονύλιο λειτουργεί σαν οξύ μέσα σε αυτή την ισορροπία, πρέπει να είναι ελαφρώς όξινο για να προσφέρει το πρωτόνιο. Αυτή η βάση, από κάθε πλευρά, πρέπει να είναι πολύ ισχυρή για να εξαναγκάσει αυτήν την ισορροπία προς αυτήν την έξοδο.
Συμπέρασμα
Οι ενόλες που ονομάζονται επίσης αλκενόλες, είναι ένα είδος αντιδραστικού μορίου ή ενδιάμεσου στη χημεία που περιγράφεται επίσης ως αλκένιο, με μόνο μια ομάδα υδροξυλίου συνδεδεμένη με τη μία πλευρά του διπλού δεσμού αλκενίου. Η αποπρωτονίωση, ή η εξάλειψη του υδρογόνου δίπλα στην καρβονυλική ομάδα όπως ένα πρωτόνιο, είναι ένα κοινό βήμα στην παραγωγή ενολών. Το αποτέλεσμα της μη επιστροφής αυτού του πρωτονίου κάπου μετά τον ειδικό για την αλληλουχία τρόπο είναι ένα ανιόν γνωστό ως ενολικό. Οι ενολικοί σχηματισμοί που απεικονίζονται είναι εννοιολογικοί. μια πιο πρόσφατη έκδοση λαμβάνει υπόψη τα τροχιακά που παράγουν και καταλαμβάνουν τα ηλεκτρόνια μέσα στο ενολικό.
Η χημική ισορροπία μεταξύ μιας κετομορφής καθώς και μιας ενόλης είναι γνωστή ως ταυτομερισμός κετο-ενόλης. Ταυτομερή υποστηρίζεται ότι υπάρχουν μεταξύ των μορφών κετο και ενόλης. Επειδή η αντίδραση των 2 τύπων απαιτεί τη μετανάστευση ενός ιόντος άλφα υδρογόνου καθώς και την αναδιάταξη ενός ζεύγους ηλεκτρονίων, αυτός ο ισομερισμός ταξινομείται ως ταυτομερισμός.