Διαμάντι
Το διαμάντι είναι ένα από τα αλλότροπα του καθαρού άνθρακα. Είναι ένα κρυσταλλικό ομοιοπολικό στερεό που βρίσκεται σε αλλουβιακά χαλίκια, σε σωλήνες κιμπερλίτη και σε παγετώνες. Εμφανίζεται σε όλα τα σχήματα και μεγέθη και βρίσκεται στη Νότια Αφρική, τη Βραζιλία, τη Ρωσία, την Αυστραλία, τις ΗΠΑ και την Ινδία. Τα ορυχεία Orapa στη Μποτσουάνα είναι τα μεγαλύτερα στον κόσμο, αλλά η Ρωσία και η Αυστραλία πρωτοστατούν στην παραγωγή διαμαντιών. Στην Ινδία, τα διαμάντια βρίσκονται στο Panna στο Madhya Pradesh και στο Golconda στην Καρνατάκα. Η λάμψη του τον κάνει τον πιο επιθυμητό πολύτιμο λίθο.
Επισκόπηση του Diamond:Natural Formation
Τα φυσικά διαμάντια βρίσκονται υπό έντονες συνθήκες θερμοκρασίας και πίεσης που προκαλούν την κρυστάλλωση των ατόμων άνθρακα. Είναι παρόν κάτω από την επιφάνεια της Γης σε βάθη 150-200 km, όπου η μέση θερμοκρασία είναι 900-1300°C και η πίεση είναι περίπου 45-60 kilobar. Σπρώχνονται στην επιφάνεια από ηφαιστειακές εκρήξεις.
Κάτω από αυτές τις έντονες συνθήκες, το λιωμένο μάγμα στον ανώτερο μανδύα της Γης διαστέλλεται με γρήγορο ρυθμό. Εκρήγνυται στην επιφάνεια της Γης με πετρώματα που φέρουν διαμάντια που ονομάζονται πετρώματα κιμπερλίτης. Ονομάζονται από τα Νοτιοαφρικανικά Ορυχεία Kimberly, όπου ανακαλύφθηκαν για πρώτη φορά.
Δομή
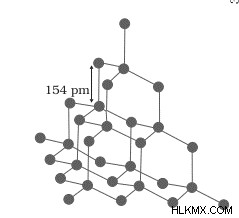
Το Diamond βασίζεται σε μια δομή κυβικού πλέγματος με επίκεντρο το πρόσωπο με επιπλέον άτομα άνθρακα μέσα στον κύβο. Τα άτομα άνθρακα υβριδίζονται sp3 και συνδέονται ομοιοπολικά με τέσσερα άλλα άτομα άνθρακα σε τετραεδρική δομή.
Ο αριθμός συντονισμού κάθε άνθρακα είναι 4. Έτσι, το διαμάντι είναι ένα γιγάντιο τρισδιάστατο μόριο στο οποίο κάθε μήκος δεσμού άνθρακα-άνθρακα είναι 154 μ.μ., σχηματίζοντας έναν ισχυρό ομοιοπολικό δεσμό. Κάθε γωνία σύνδεσης είναι 109,5°.
Τεχνητή προετοιμασία
Ο γραφίτης χρησιμοποιείται για την κατασκευή συνθετικών ή τεχνητών διαμαντιών. Όταν υποβάλλεται σε πολύ υψηλή πίεση και υψηλές θερμοκρασίες (HPHT) περίπου 3000°C, ο γραφίτης μετατρέπεται σε διαμάντια.
Είναι φυσικά και χημικά παρόμοια με τα φυσικά σε σύνθεση, κρυστάλλωση και ισοτροπική μορφή. Η μόνη διαφορά είναι ότι τα συνθετικά στερεά που παράγονται κάτω από τέτοιες συνθήκες είναι μάλλον μικρά.
Φυσικές και χημικές ιδιότητες
- Στην καθαρή τους μορφή, τα διαμάντια είναι διαφανή και άχρωμα. Οι ακαθαρσίες τους δίνουν χρώματα.
- Τα διαμάντια είναι σκληρά αλλά και εύθραυστα.
- Λόγω της ικανότητάς τους να αντανακλούν το φως, έχουν την υψηλότερη μη μεταλλική λάμψη.
- Το διαμάντι έχει δείκτη διάθλασης 2,5, που το κάνει να αστράφτει.
- Έχει επίσης σχετικά υψηλή διασπορά. Όσο υψηλότερη είναι η τιμή διασποράς, τόσο πιο πολύχρωμα φλας μπορεί να εμφανίσει το διαμάντι.
- Έχει μέση πυκνότητα 3,5 g/cm3.
- Είναι αδιάλυτο σε οποιονδήποτε διαλύτη.
- Αν και το διαμάντι μπορεί να αντέξει τη θερμότητα, η παρατεταμένη θέρμανση μπορεί να το μετατρέψει σε γραφίτη.
- Καίει στον αέρα στους 900°C για να σχηματίσει διοξείδιο του άνθρακα.
- Σε θερμοκρασία δωματίου, είναι ένας από τους καλύτερους θερμικούς αγωγούς.
Με βάση τη δομή, οι χαρακτηριστικές ιδιότητες ενός διαμαντιού μπορούν να εξηγηθούν ως εξής:
- Σκληρότητα:Καθώς οι δεσμοί άνθρακα-άνθρακα είναι πολύ ισχυροί ομοιοπολικοί δεσμοί, το διαμάντι είναι σκληρό και έχει υψηλή πυκνότητα. Είναι η πιο σκληρή ουσία που απαντάται στη φύση. Τα μαύρα είναι τα πιο σκληρά από όλα.
- Σημείο τήξης:Το σημείο τήξεώς του είναι 3600°C, το οποίο είναι πολύ υψηλό. Αυτό συμβαίνει επειδή η τήξη του διαμαντιού απαιτεί το σπάσιμο των ισχυρών ομοιοπολικών δεσμών του.
- Κακός αγωγός:Όλα τα ηλεκτρόνια σθένους του διαμαντιού εμπλέκονται στη σύνδεση, χωρίς να αφήνουν ελεύθερα ηλεκτρόνια να μεταφέρουν ηλεκτρικά ρεύματα. Ως εκ τούτου, είναι κακός αγωγός του ηλεκτρισμού.
Αξία ως διαμάντι
Η αξία ενός διαμαντιού ως διαμάντι εξαρτάται από το βάρος και τις ακαθαρσίες του. Τα 4C καθορίζουν την ποιότητα ενός διαμαντιού:χρώμα, κοπή, διαύγεια και βάρος σε καράτι. Το βάρος του εκφράζεται σε καράτια [1 καράτι =0,2 g].
Τα άχρωμα, διαφανή διαμάντια είναι τα πιο ακριβά επειδή έχουν αμελητέα ακαθαρσίες. Είναι επίσης τέλεια γυαλισμένα για να είναι ιδιαίτερα ανακλαστικά και να αστράφτουν περισσότερο. Η αξία ενός διαμαντιού μειώνεται με την αύξηση των ακαθαρσιών του.
Τύποι
Είναι η παρουσία μικρών ιχνών μεταλλικού οξειδίου και αλατιού που προσδίδει ξεχωριστά χρώματα στα διαμάντια. Τα πιο σκούρα χρώματα, δηλαδή κόκκινο, ροζ και μπλε, είναι εξαιρετικά σπάνια. Τα διαμάντια μπορεί επίσης να είναι γκρι, κίτρινα, καφέ, πράσινα, πορτοκαλί, ακόμη και μαύρα.
Τα μαύρα διαμάντια έχουν ακαθαρσίες οξειδίου του χαλκού. Δεν χρησιμοποιούνται ως πολύτιμοι λίθοι, αλλά έχουν σημαντικές βιομηχανικές χρήσεις.
Χρησιμοποιήσεις
Τα αγνά διαμάντια χρησιμοποιούνται ως πολύτιμοι λίθοι στα κοσμήματα λόγω της λαμπρής λάμψης τους.
Χρησιμοποιούνται ακάθαρτα ή συνθετικά διαμάντια:
- Για κοπή και διάτρηση πετρωμάτων, γυαλιού ή άλλων διαμαντιών.
- Ως κεφαλές κορυφής σε τρυπάνια βαθιάς διάτρησης.
- Ως ρουλεμάν σε ρολόγια.
- Ως βελόνες για πικάπ που παίζουν πολύ.
- Για την κατασκευή παραθύρων με προστασία από την ακτινοβολία για διαστημικούς δορυφόρους.
Συμπέρασμα
Τα διαμάντια είναι κρυσταλλικά ομοιοπολικά στερεά από καθαρό άνθρακα. Στη φύση, σχηματίζονται για εκατομμύρια χρόνια κάτω από ακραίες συνθήκες πίεσης και θερμοκρασίας. Συνθετικά, το διαμάντι σχηματίζεται από γραφίτη χρησιμοποιώντας τη μέθοδο HPHT. Έχει μια επικεντρωμένη δομή κυβικού πλέγματος με sp3 υβριδισμένα άτομα άνθρακα, το καθένα ομοιοπολικά συνδεδεμένο με τέσσερα περιβάλλοντα άτομα, χωρίς να αφήνει ελεύθερο ηλεκτρόνιο.
Λόγω της δομής του, είναι η πιο σκληρή ουσία που απαντάται στη φύση, με υψηλό σημείο τήξης. Είναι εξαιρετικός θερμικός αγωγός αλλά κακός ηλεκτρικός μονωτήρας. Καίγεται στον αέρα στους 900°C για να σχηματίσει διοξείδιο του άνθρακα.
Το διαμάντι αστράφτει λόγω του υψηλού δείκτη διάθλασης και της ισχύος διασποράς του. Είναι πιο δημοφιλές ως πολύτιμος λίθος, αλλά χρησιμοποιείται επίσης για την κοπή άλλων διαμαντιών και την κατασκευή παραθύρων ανθεκτικών στην ακτινοβολία για διαστημικούς δορυφόρους.