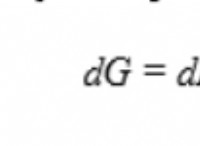Οι μαθηματικές μέθοδοι βοηθούν στην εξήγηση γιατί τα υγρά μέταλλα έχουν άγρια διαφορετικά σημεία θραύσης
επιφανειακή τάση και τριχοειδή αποτελέσματα
Η επιφανειακή τάση αποτελεί βασικό παράγοντα για τον προσδιορισμό του σημείου θραύσης ενός υγρού μετάλλου. Είναι η δύναμη που προκαλεί τη σύναψη της επιφάνειας ενός υγρού και την ελαχιστοποίηση της επιφάνειας του. Όσο υψηλότερη είναι η επιφανειακή τάση, τόσο πιο ανθεκτικό είναι το υγρό να σπάσει.
Στα υγρά μέταλλα, η επιφανειακή τάση προκύπτει λόγω των ισχυρών μεταλλικών δεσμών μεταξύ των ατόμων. Αυτοί οι δεσμοί δημιουργούν μια συνεκτική δύναμη που συγκρατεί το υγρό μαζί και αντιστέκεται στη διάλυση. Η επιφανειακή τάση των υγρών μετάλλων είναι συνήθως πολύ υψηλότερη από αυτή των άλλων υγρών, όπως το νερό ή το λάδι.
τριχοειδή εφέ
Οι τριχοειδείς επιδράσεις είναι επίσης ζωτικής σημασίας για την κατανόηση του σημείου θραύσης των υγρών μετάλλων. Οι τριχοειδείς επιδράσεις εμφανίζονται όταν ένα υγρό έρχεται σε επαφή με μια συμπαγή επιφάνεια. Το υγρό τείνει να ανεβαίνει ή να πέφτει κατά μήκος της επιφάνειας, ανάλογα με τις ιδιότητες διαβροχής του υγρού και του στερεού.
Στα υγρά μέταλλα, τα τριχοειδή αποτελέσματα μπορούν να οδηγήσουν στο σχηματισμό λεπτών υγρών γεφυρών μεταξύ δύο στερεών επιφανειών. Αυτές οι γέφυρες σταθεροποιούνται με επιφανειακή τάση και μπορούν να υποστηρίξουν ένα σημαντικό βάρος. Ωστόσο, εάν το βάρος υπερβαίνει μια κρίσιμη τιμή, η υγρή γέφυρα θα σπάσει, προκαλώντας τη διαχωρισμό του υγρού μετάλλου.
Μαθηματική μοντελοποίηση
Τα μαθηματικά μοντέλα έχουν αναπτυχθεί για να προβλέψουν το σημείο θραύσης των υγρών μετάλλων με βάση την επιφανειακή τάση και τα τριχοειδή αποτελέσματα. Αυτά τα μοντέλα συνήθως περιλαμβάνουν την επίλυση διαφορικών εξισώσεων που περιγράφουν τη δυναμική της διεπαφής υγρού-στερεού.
Μια κοινή προσέγγιση είναι να χρησιμοποιηθεί η εξίσωση νεαρής διάλυσης, η οποία σχετίζεται με τη διαφορά πίεσης σε μια διεπαφή με καμπύλη υγρού-αερίου στην επιφανειακή τάση και την καμπυλότητα της διεπαφής. Με την εφαρμογή αυτής της εξίσωσης σε μια υγρή γέφυρα, είναι δυνατόν να υπολογιστεί το κρίσιμο βάρος που προκαλεί τη διάσπαση της γέφυρας.
Μια άλλη προσέγγιση περιλαμβάνει τη χρήση των εξισώσεων Navier-Stokes, οι οποίες περιγράφουν την κίνηση των ιξώδους υγρών. Αυτές οι εξισώσεις μπορούν να χρησιμοποιηθούν για την προσομοίωση της ροής του υγρού μετάλλου γύρω από τις στερεές επιφάνειες και την πρόβλεψη του σχηματισμού και διάλυσης υγρών γέφυρων.
Συμπέρασμα
Οι μαθηματικές μέθοδοι παρέχουν ένα ισχυρό εργαλείο για την κατανόηση του σημείου θραύσης των υγρών μετάλλων. Λαμβάνοντας υπόψη την επιφανειακή τάση, τις τριχοειδείς επιδράσεις και τη δυναμική των υγρών, είναι δυνατόν να αναπτυχθούν μοντέλα που προβλέπουν με ακρίβεια τις συνθήκες υπό τις οποίες παραβιάζουν τα υγρά μέταλλα. Αυτή η γνώση είναι απαραίτητη για διάφορες εφαρμογές που περιλαμβάνουν υγρά μέταλλα, όπως μεταλλικές εργασίες, χύτευση και μικρορευστές.