Πώς γίνεται ένα άτομο σταθερό;
1. Ολοκλήρωση του εξωτερικού ηλεκτρονικού κελύφους (κανόνας οκτάδων):
Ο "κανόνας οκτάδων" ή ο "κανόνας του ντουέτου" αναφέρει ότι τα άτομα τείνουν να κερδίζουν, να χάνουν ή να μοιράζονται ηλεκτρόνια προκειμένου να επιτευχθούν μια σταθερή διαμόρφωση ηλεκτρονίων, έχοντας ένα πλήρες εξώτατο κέλυφος ηλεκτρονίων. Αυτό έχει ως αποτέλεσμα μια πιο σταθερή και χαμηλότερη ενεργειακή κατάσταση για το άτομο. Για παράδειγμα:
- Το νάτριο (Na) έχει ένα ηλεκτρόνιο στο εξωτερικό του κέλυφος. Επιτυγχάνει σταθερότητα χάνοντας αυτό το ηλεκτρόνιο, με αποτέλεσμα ένα πλήρες εξώτατο κέλυφος ηλεκτρονίων με μια διαμόρφωση ευγενών αερίου (NE).
- Το χλώριο (CL) έχει επτά ηλεκτρόνια στο εξωτερικό κέλυφος του. Γίνεται σταθερό κερδίζοντας ένα ηλεκτρόνιο για να ολοκληρώσει το εξώτατο κέλυφος ηλεκτρονίων του, επιτυγχάνοντας την ίδια διαμόρφωση με ένα ευγενές αέριο (AR).
2. Δημιουργία χημικών δεσμών:
Τα άτομα μπορούν επίσης να επιτύχουν σταθερότητα σχηματίζοντας χημικούς δεσμούς με άλλα άτομα. Η χημική σύνδεση περιλαμβάνει την κοινή χρήση ή τη μεταφορά ηλεκτρονίων μεταξύ των ατόμων, με αποτέλεσμα μια πιο σταθερή διαμόρφωση για τα συνδεδεμένα άτομα. Υπάρχουν διάφοροι τύποι χημικών δεσμών, όπως:
- Ιονικοί δεσμοί:Σε ιοντική συγκόλληση, ένα άτομο χάνει ηλεκτρόνια, ενώ ένα άλλο κερδίζει ηλεκτρόνια, με αποτέλεσμα το σχηματισμό αντίθετα φορτισμένων ιόντων. Η ηλεκτροστατική έλξη μεταξύ αυτών των ιόντων συγκρατεί την ένωση, δημιουργώντας σταθερότητα.
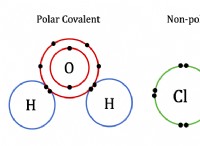
- ομοιοπολικοί δεσμοί:Η ομοιοπολική συγκόλληση περιλαμβάνει την κατανομή των ζευγών ηλεκτρονίων μεταξύ των ατόμων. Αυτή η κοινή χρήση ηλεκτρονίων έχει ως αποτέλεσμα μια σταθερή διαμόρφωση ηλεκτρονίων για κάθε άτομο.
- Μεταλλικοί δεσμοί:Στη μεταλλική σύνδεση, τα ηλεκτρόνια μοιράζονται μεταξύ πολλών μεταλλικών ατόμων, σχηματίζοντας μια "θάλασσα" ηλεκτρονίων που συγκρατούν το μεταλλικό πλέγμα μαζί, παρέχοντας δύναμη και σταθερότητα.
Με την επίτευξη ενός πλήρους εξωτερικού κελύφους ηλεκτρονίων ή σχηματίζοντας χημικούς δεσμούς, τα άτομα επιτυγχάνουν χαμηλότερη ενεργειακή κατάσταση και γίνονται σταθερές.