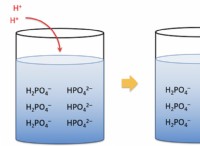
Πώς συμπεριφέρονται τα σωματίδια σε μια λύση;
1. Brownian Motion:Τα σωματίδια σε ένα διάλυμα υφίστανται συνεχή τυχαία κίνηση γνωστή ως κίνηση Brownian. Αυτή η κίνηση προκαλείται από συγκρούσεις μεταξύ των σωματιδίων και των μορίων διαλύτη. Καθώς τα σωματίδια μειώνονται σε μέγεθος, η κίνηση τους Brownian γίνεται πιο έντονη.
2. Διάχυση:Λόγω της κίνησης Brownian, τα σωματίδια εξαπλώνονται και διανέμονται ομοιόμορφα καθ 'όλη τη διάρκεια του διαλύματος με την πάροδο του χρόνου. Αυτή η διαδικασία ονομάζεται διάχυση. Πρόκειται για μια παθητική κίνηση που οδηγείται από τη βαθμίδα συγκέντρωσης των σωματιδίων.
3. Καθίζηση:μεγαλύτερα σωματίδια ή μόρια σε ένα διάλυμα μπορεί να παρουσιάσουν καθίζηση, η οποία είναι η καθίζηση των σωματιδίων υπό την επίδραση της βαρύτητας. Η καθίζηση συμβαίνει όταν η βαρυτική δύναμη που δρουν στα σωματίδια είναι μεγαλύτερη από τις αντίπαλες δυνάμεις, όπως η κίνηση και οι συγκρούσεις του Brownian.
4. Όσμωση:Η όσμωση αναφέρεται στην κίνηση των μορίων διαλύτη σε μια ημιπερατή μεμβράνη από μια περιοχή χαμηλότερης συγκέντρωσης διαλυτής ουσίας σε μια περιοχή υψηλότερης συγκέντρωσης διαλυτής ουσίας. Αυτή η διαδικασία συμβαίνει σε απόκριση της κλίσης της συγκέντρωσης των σωματιδίων διαλυμένης ουσίας, με στόχο την εξίσωση της συγκέντρωσης της διαλυμένης ουσίας και στις δύο πλευρές της μεμβράνης.
5. Η πήξη και η κροκίδωση:κολλοειδή σωματίδια σε ένα διάλυμα μπορεί να υποβληθούν σε πήξη ή κροκίδωση. Η πήξη περιλαμβάνει τη συσσωμάτωση των σωματιδίων λόγω των αξιοθέατων μεταξύ των σωματιδίων, ενώ η κροκίδωση αναφέρεται στον σχηματισμό χαλαρών, ανοικτών δομών που ονομάζονται flocs. Η πήξη και η κροκίδωση επηρεάζονται από παράγοντες όπως το μέγεθος των σωματιδίων, το φορτίο και η παρουσία ηλεκτρολυτών.
6. Ενυδάτωση και διαλυτοποίηση:Όταν ένα σωματίδιο διαλυμένης ουσίας διαλύεται σε έναν διαλύτη, αλληλεπιδρά με τα περιβάλλοντα μόρια διαλύτη. Για παράδειγμα, σε ένα υδατικό διάλυμα, τα μόρια νερού σχηματίζουν δεσμούς υδρογόνου με τις πολικές ομάδες στα σωματίδια διαλυτής ουσίας. Αυτή η διαδικασία ονομάζεται ενυδάτωση ή διαλυτοποίηση. Η έκταση της ενυδάτωσης ή της διαλυτοποίησης επηρεάζει τη διαλυτότητα και τη συμπεριφορά των σωματιδίων στο διάλυμα.
7. Οι ηλεκτροστατικές αλληλεπιδράσεις:τα φορτισμένα σωματίδια σε ένα διάλυμα αλληλεπιδρούν μέσω ηλεκτροστατικών δυνάμεων. Τα θετικά φορτισμένα σωματίδια (κατιόντα) προσελκύονται από αρνητικά φορτισμένα σωματίδια (Anions), οδηγώντας στο σχηματισμό ζεύγους ιόντων ή πιο σύνθετες δομές. Αυτές οι ηλεκτροστατικές αλληλεπιδράσεις διαδραματίζουν κρίσιμο ρόλο στη σταθερότητα, την αντιδραστικότητα και τη συμπεριφορά των φορτισμένων σωματιδίων στο διάλυμα.
8. Χημικές αντιδράσεις:Τα σωματίδια σε ένα διάλυμα μπορούν να υποβληθούν σε διάφορες χημικές αντιδράσεις μεταξύ τους ή με τα μόρια του διαλύτη. Αυτές οι αντιδράσεις μπορούν να οδηγήσουν στον σχηματισμό νέων ενώσεων, στην κατακρήμνιση των αδιάλυτων προϊόντων ή στις αλλαγές στις ιδιότητες του διαλύματος.
Η κατανόηση της συμπεριφοράς των σωματιδίων σε μια λύση είναι απαραίτητη για πολλούς τομείς της επιστήμης, όπως η χημεία, η φυσική, η βιολογία, η επιστήμη των υλικών και η περιβαλλοντική επιστήμη. Βοηθά στην πρόβλεψη των φυσικών και χημικών ιδιοτήτων των λύσεων, στο σχεδιασμό και τη βελτιστοποίηση των διαδικασιών που περιλαμβάνουν λύσεις και στην κατανόηση των αλληλεπιδράσεων και της δυναμικής των σωματιδίων σε μικροσκοπικό επίπεδο.