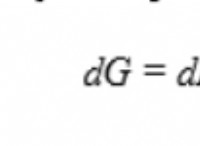Ποιο είναι το κατά προσέγγιση κατάθλιψη σημείου κατάψυξης 0,020m υδατικό διάλυμα NABR;
Κατανόηση της κατάθλιψης σημείου κατάψυξης
Η κατάθλιψη σημείων κατάψυξης είναι μια περιεκτική ιδιότητα, που σημαίνει ότι εξαρτάται από τη συγκέντρωση σωματιδίων διαλυτής ουσίας σε ένα διάλυμα και όχι την ταυτότητά τους. Ο τύπος για την κατάθλιψη του σημείου κατάψυξης είναι:
Δt
όπου:
* Δt
* K
* m είναι η μολικότητα του διαλύματος
* I είναι ο παράγοντας van't hoff, που αντιπροσωπεύει τον αριθμό των ιόντων που κάθε μονάδα τύπου της διαλυμένης ουσίας διαχωρίζεται σε διάλυμα.
Υπολογισμοί
1. k
2. Molality (m): Έχετε παράσχει τη μολικότητα του διαλύματος ως 0,020 m.
3. Το NABR διαχωρίζεται σε δύο ιόντα σε διάλυμα (na
Βάζοντας όλα μαζί:
Δt
Δt
Συμπέρασμα
Η κατάθλιψη κατά προσέγγιση κατάψυξης ενός υδατικού διαλύματος NABR 0,020 Μ είναι περίπου 0,074 ° C . Αυτό σημαίνει ότι το σημείο κατάψυξης του διαλύματος θα είναι περίπου 0,074 ° C χαμηλότερο από το σημείο κατάψυξης του καθαρού νερού (0 ° C).