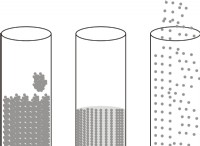
Πότε εξατμίζεται μια ουσία;
* Διαμοριακές δυνάμεις: Αυτές είναι οι ελκυστικές δυνάμεις μεταξύ των μορίων, όπως η συγκόλληση υδρογόνου, οι αλληλεπιδράσεις διπόλης-δίπολου και οι δυνάμεις διασποράς του Λονδίνου. Διατηρούν μόρια μαζί σε ένα υγρό.
* Κινητική ενέργεια: Τα μόρια κινούνται συνεχώς και δονούν. Η θερμότερη είναι μια ουσία, τόσο ταχύτερα τα μόρια του κινούνται και η πιο κινητική ενέργεια που έχουν.
* εξάτμιση: Όταν ένα μόριο στην επιφάνεια ενός υγρού κερδίζει αρκετή κινητική ενέργεια, μπορεί να ξεπεράσει τις διαμοριακές δυνάμεις που την κρατάει στο υγρό. Στη συνέχεια σπάει ελεύθερο και εισέρχεται στην αέρια φάση.
Παράγοντες που επηρεάζουν την εξάτμιση:
* Θερμοκρασία: Οι υψηλότερες θερμοκρασίες σημαίνουν περισσότερη κινητική ενέργεια, καθιστώντας την εξάτμιση ταχύτερη.
* επιφάνεια: Μια μεγαλύτερη επιφάνεια εκθέτει περισσότερα μόρια στον αέρα, αυξάνοντας το ρυθμό εξάτμισης.
* Κίνηση αέρα: Ο κινούμενος αέρας μεταφέρει τα απομακρυσμένα μόρια εξατμισμένα, μειώνοντας τη συγκέντρωση μορίων αερίου πάνω από το υγρό και ενθαρρύνοντας την περαιτέρω εξάτμιση.
* Τύπος ουσίας: Οι διαφορετικές ουσίες έχουν διαφορετικές διαμοριακές δυνάμεις, επηρεάζοντας τα ποσοστά εξάτμισης τους. Οι ουσίες με αδύναμες διαμοριακές δυνάμεις εξατμίζονται πιο εύκολα.
Συνοπτικά: Η εξάτμιση είναι μια συνεχής διαδικασία όπου τα μόρια κερδίζουν αρκετή ενέργεια για να ξεφύγουν από την υγρή κατάσταση και να γίνουν αέριο. Αυτή η διαδικασία επηρεάζεται από διάφορους παράγοντες, συμπεριλαμβανομένης της θερμοκρασίας, της επιφάνειας, της κίνησης του αέρα και της φύσης της ίδιας της ουσίας.