Τι υγρά μπορούν να αναμειχθούν με νερό;
υγρά που αναμειγνύονται καλά με νερό (αναμίξιμο):
* αλκοόλες: Αιθανόλη (αλκοόλ), μεθανόλη, ισοπροπανόλη
* οξέα: Ξίδι (οξικό οξύ), χυμό λεμονιού (κιτρικό οξύ), υδροχλωρικό οξύ
* βάσεις: Διάλυμα αμμωνίας, διάλυμα υδροξειδίου του νατρίου
* Ορισμένα άλατα: Επιτραπέζιο αλάτι (χλωριούχο νάτριο), ζάχαρη (σακχαρόζη)
υγρά που δεν αναμειγνύονται καλά με νερό (μη αναμίξιμο):
* Λάδια: Φυτικό έλαιο, ορυκτέλαιο, ελαιόλαδο
* βενζίνη
* κηροζίνη
* Mercury
Είναι σημαντικό να σημειώσετε:
* Διαλυτότητα: Ακόμη και τα αναμίξιμα υγρά έχουν όρια για το πόσο μπορεί να διαλυθεί στο νερό. Για παράδειγμα, μπορείτε να διαλύσετε πολλή ζάχαρη στο νερό, αλλά τελικά, το νερό θα γίνει κορεσμένο και δεν θα διαλυθεί περισσότερη ζάχαρη.
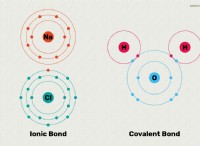
* πολικότητα: Το νερό είναι ένα πολικό μόριο, που σημαίνει ότι έχει θετικό και αρνητικό τέλος. Τα υγρά που είναι επίσης πολικά τείνουν να αναμειγνύονται καλά με νερό. Τα μη πολικά υγρά, όπως τα έλαια, δεν αναμιγνύονται καλά με νερό.
Επιτρέψτε μου να ξέρω αν θέλετε περισσότερες λεπτομέρειες σχετικά με συγκεκριμένα υγρά!