Όταν λαμβάνει χώρα μια χημική αντίδραση;
Τι συμβαίνει κατά τη διάρκεια μιας χημικής αντίδρασης:
* Αντιδραστήρια: Οι αρχικές ουσίες σε μια αντίδραση ονομάζονται αντιδραστήρια.
* Προϊόντα: Οι νέες ουσίες που σχηματίζονται ονομάζονται προϊόντα.
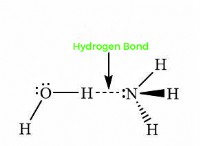
* Χημικοί δεσμοί: Τα άτομα συγκρατούνται μαζί σε μόρια με χημικούς δεσμούς. Αυτά τα ομόλογα αποθηκεύουν ενέργεια.
* Breaking Bonds: Για να σχηματίσουν νέα προϊόντα, τα ομόλογα στα αντιδραστήρια πρέπει να σπάσουν. Αυτό απαιτεί εισροή ενέργειας.
* σχηματίζοντας ομόλογα: Τα νέα ομόλογα σχηματίζονται μεταξύ των ατόμων για τη δημιουργία των προϊόντων. Αυτό απελευθερώνει ενέργεια.
συνθήκες για μια αντίδραση που συμβαίνει:
* σύγκρουση: Τα μόρια αντιδραστηρίων πρέπει να συγκρούονται μεταξύ τους με επαρκή ενέργεια.
* Ενέργεια ενεργοποίησης: Αυτή είναι η ελάχιστη ενέργεια που απαιτείται για να ξεκινήσει μια αντίδραση.
* Ευνοϊκές συνθήκες: Ορισμένες αντιδράσεις χρειάζονται συγκεκριμένες καταστάσεις όπως η θερμότητα, το φως ή οι καταλύτες.
Παραδείγματα χημικών αντιδράσεων:
* καύση ξύλου: Το ξύλο (αντιδραστήριο) αντιδρά με οξυγόνο (αντιδραστήριο) παρουσία θερμότητας για να παράγει τέφρα, διοξείδιο του άνθρακα και νερό (προϊόντα).
* σκουριά: Ο σίδηρος (αντιδραστήριο) αντιδρά με οξυγόνο (αντιδραστήριο) παρουσία νερού για να σχηματίσει σκουριά (προϊόν).
* φωτοσύνθεση: Τα φυτά χρησιμοποιούν το φως του ήλιου (ενέργεια) για να μετατρέψουν το διοξείδιο του άνθρακα και το νερό (αντιδραστήρια) σε γλυκόζη και οξυγόνο (προϊόντα).
Βασικά σημεία:
* Οι χημικές αντιδράσεις περιλαμβάνουν τη δημιουργία νέων ουσιών με διαφορετικές ιδιότητες από τα αντιδραστήρια.
* Η ενέργεια είτε απορροφάται είτε απελευθερώνεται κατά τη διάρκεια χημικής αντίδρασης.
* Ο ρυθμός αντίδρασης μπορεί να επηρεαστεί από παράγοντες όπως η θερμοκρασία, η συγκέντρωση και η παρουσία ενός καταλύτη.