Η χρήση των κανόνων διαλυτότητας προβλέπει εάν η ένωση θα ήταν διαλυτή ή όχι μαγγάνιο 2 χλωριούχο a διαλυτό b διαλυτό;
Εδώ είναι γιατί:
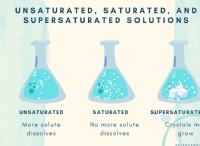
* Κανόνες διαλυτότητας: Οι κανόνες διαλυτότητας είναι ένα σύνολο κατευθυντήριων γραμμών που χρησιμοποιούνται για να προβλέψουν εάν μια ένωση θα διαλυθεί στο νερό.
* Χλωρίδια: Τα περισσότερα χλωρίδια είναι διαλυτά, με τις αξιοσημείωτες εξαιρέσεις του χλωριούχου αργύρου (AGCL), του χλωριούχου μολύβδου (II) (PBCL₂) και του χλωριούχου υδραργύρου (I) (HG₂CL₂).
* μαγγάνιο (ii): Το μαγγάνιο (II) δεν είναι μία από τις εξαιρέσεις από τον κανόνα για τη διαλυτότητα χλωριδίου.
Επομένως, το χλωριούχο μαγγάνιο (II) (MnCl₂) είναι διαλυτό στο νερό.