Η δέσμευση υδρογόνου συμβαίνει σε μόρια όπου το υδρογόνο συνδέεται με τα στοιχεία του αζώτου αζώτου άνθρακα φθορίου;
Εδώ είναι γιατί:
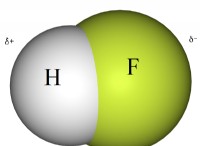
* Υψηλή ηλεκτροαρνητικότητα: Αυτά τα τρία στοιχεία έχουν υψηλή ηλεκτροαρνητικότητα, που σημαίνει ότι προσελκύουν έντονα ηλεκτρόνια. Όταν συνδέονται με υδρογόνο, τα κοινόχρηστα ηλεκτρόνια περνούν περισσότερο χρόνο γύρω από το άτομο φθορίου, οξυγόνου ή αζώτου, δημιουργώντας ένα μερικό αρνητικό φορτίο (δ-) σε αυτό το άτομο και ένα μερικό θετικό φορτίο (δ+) στο άτομο υδρογόνου.
* Ισχυρή διπολική στιγμή: Αυτή η ανομοιόμορφη κατανομή των ηλεκτρονίων δημιουργεί μια ισχυρή διπολική στιγμή, με το θετικό άκρο του δίπολο στο άτομο υδρογόνου και το αρνητικό άκρο στο άτομο φθορίου, οξυγόνου ή αζώτου.
* σχηματισμός δεσμών υδρογόνου: Το θετικό άτομο υδρογόνου σε ένα μόριο μπορεί στη συνέχεια να σχηματίσει μια ισχυρή ηλεκτροστατική έλξη (δεσμός υδρογόνου) με το αρνητικό άτομο οξυγόνου, φθορίου ή αζώτου ενός άλλου μορίου.
βόριο δεν συμμετέχει στη δέσμευση υδρογόνου. Ενώ είναι λιγότερο ηλεκτροαρνητικό από τα άλλα στοιχεία που αναφέρονται, δεν σχηματίζουν αρκετά ισχυρά δίπολα για να δημιουργήσουν τις απαραίτητες αλληλεπιδράσεις για τη δέσμευση υδρογόνου.