Ποια είναι η εξίσωση για το υδροχλωρικό οξύ αλουμινίου και το υδροχλωρικό οξύ;
2Al (s) + 6hcl (aq) → 2alcl₃ (aq) + 3H₂ (g)
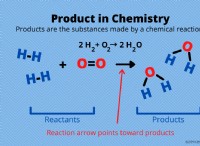
Ακολουθεί μια ανάλυση της αντίδρασης:
* 2Al (s): Αυτό αντιπροσωπεύει δύο γραμμομορείς στερεού αλουμινίου.
* 6hcl (aq): Αυτό αντιπροσωπεύει έξι γραμμομονείς υδροχλωρικού οξέος σε υδατικό διάλυμα.
* 2alcl₃ (aq): Αυτό αντιπροσωπεύει δύο γραμμομορείς χλωριούχου αλουμινίου, το οποίο διαλύεται στο διάλυμα.
* 3H₂ (g): Αυτό αντιπροσωπεύει τρεις γραμμομορείς αερίου υδρογόνου, το οποίο απελευθερώνεται ως φυσαλίδες.
Επεξήγηση:
Αυτή η αντίδραση είναι μια ενιαία αντίδραση μετατόπισης όπου το αλουμίνιο (AL) είναι πιο αντιδραστική από το υδρογόνο (Η). Το αλουμίνιο μετατοπίζει το υδρογόνο από το υδροχλωρικό οξύ, σχηματίζοντας χλωριούχο αλουμινίου (ALCL₃) και απελευθερώνοντας αέριο υδρογόνου (Η).
Αυτή η αντίδραση είναι επίσης εξωθερμική, που σημαίνει ότι απελευθερώνει θερμότητα και μπορεί να παρατηρηθεί από την εξέλιξη της θερμότητας και τον σχηματισμό φυσαλίδων.