Είναι το θείο πιο αντιδραστικό από το άζωτο;
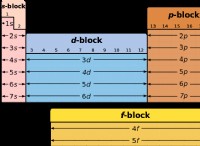
* Διαμόρφωση ηλεκτρονίων: Το Sulphur διαθέτει έξι ηλεκτρόνια σθένους, καθιστώντας πιο πιθανό να κερδίσει δύο ηλεκτρόνια για να επιτύχει μια σταθερή διαμόρφωση οκτάδων. Το άζωτο, με πέντε ηλεκτρόνια σθένους, πρέπει να κερδίσει τρία ηλεκτρόνια, τα οποία απαιτούν περισσότερη ενέργεια.
* Ηλεκτροργατιστικότητα: Το θείο είναι λιγότερο ηλεκτροαρνητικό από το άζωτο. Αυτό σημαίνει ότι το θείο είναι πιο πρόθυμο να χάσει ηλεκτρόνια και να συμμετέχει σε χημικές αντιδράσεις.
* Αντοχή δεσμού: Ο τριπλός δεσμός Ν-Ν σε αέριο αζώτου (N₂) είναι απίστευτα ισχυρός, καθιστώντας το άζωτο πολύ μη αντιδραστικό. Το θείο, από την άλλη πλευρά, σχηματίζει ασθενέστερους δεσμούς S-S.
* καταστάσεις οξείδωσης: Το θείο παρουσιάζει ευρύτερο φάσμα καταστάσεων οξείδωσης από το άζωτο, υποδεικνύοντας μεγαλύτερη τάση για να κερδίσει ή να χάσει ηλεκτρόνια.
Ωστόσο, είναι σημαντικό να σημειωθεί ότι η αντιδραστικότητα εξαρτάται από συγκεκριμένες συνθήκες:
* Θερμοκρασία: Το άζωτο μπορεί να γίνει εξαιρετικά αντιδραστικό σε εξαιρετικά υψηλές θερμοκρασίες.
* Παρουσία καταλυτών: Ειδικοί καταλύτες μπορούν να προωθήσουν αντιδράσεις που περιλαμβάνουν άζωτο.
Συνολικά, υπό κανονικές συνθήκες, το θείο θεωρείται πιο αντιδραστικό από το άζωτο λόγω της ηλεκτρονικής δομής και των ιδιοτήτων συγκόλλησης.