Γιατί το θείο έχει μεγάλο ατομικό μέγεθος από το μαγνήσιο;
* Ατομικός αριθμός: Το θείο έχει ατομικό αριθμό 16, που σημαίνει ότι έχει 16 πρωτόνια στον πυρήνα του. Το μαγνήσιο έχει ατομικό αριθμό 12, που σημαίνει ότι έχει 12 πρωτόνια.
* Διαμόρφωση ηλεκτρονίων: Το Sulphur έχει τη διαμόρφωση ηλεκτρονίων [NE] 3S2 3p⁴, ενώ το μαγνήσιο έχει [NE] 3S2. Και τα δύο στοιχεία έχουν τα εξωτερικά τους ηλεκτρόνια στο τρίτο επίπεδο ενέργειας (n =3).
* Αποτελεσματικό πυρηνικό φορτίο: Παρά την ίδια περίοδο, το θείο έχει υψηλότερο αποτελεσματικό πυρηνικό φορτίο (το καθαρό θετικό φορτίο που βιώνει ένα ηλεκτρόνιο) από το μαγνήσιο. Αυτό οφείλεται στο γεγονός ότι το θείο έχει περισσότερα πρωτόνια στον πυρήνα του που προσελκύει τα ηλεκτρόνια του πιο έντονα.
* Εφέ θωράκισης: Τα ηλεκτρόνια στα εσωτερικά κελύφη (n =1 και n =2) προστατεύουν τα εξωτερικά ηλεκτρόνια από το πλήρες θετικό φορτίο του πυρήνα. Το αποτέλεσμα θωράκισης είναι περίπου το ίδιο και για τα δύο στοιχεία.
Επομένως:
* Το υψηλότερο αποτελεσματικό πυρηνικό φορτίο στο θείο τραβά τα ηλεκτρόνια του πιο κοντά στον πυρήνα, οδηγώντας σε μικρότερη ατομική ακτίνα.
* Το ασθενέστερο αποτελεσματικό πυρηνικό φορτίο του μαγνησίου επιτρέπει στα ηλεκτρόνια του να εξαπλωθούν περισσότερο, με αποτέλεσμα μια μεγαλύτερη ατομική ακτίνα.
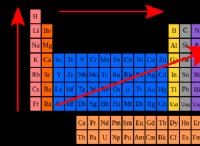
Γενικά, καθώς μετακινείτε σε μια περίοδο από αριστερά προς τα δεξιά, το ατομικό μέγεθος μειώνεται λόγω του αυξανόμενου αποτελεσματικού πυρηνικού φορτίου που τραβά τα ηλεκτρόνια πιο κοντά στον πυρήνα.