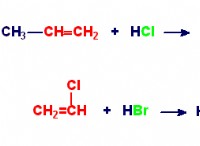
Γιατί χρησιμοποιήθηκε ένα συμπυκνωμένο διάλυμα εάν δεν υπάρχει αντίδραση με το αραιό διάλυμα;
* Η αυξημένη συγκέντρωση σημαίνει περισσότερο αντιδραστήριο: Ένα συμπυκνωμένο διάλυμα συσκευάζει περισσότερα μόρια αντιδραστηρίου στον ίδιο όγκο. Αυτό μπορεί:
* Ξεκινήστε την ενέργεια ενεργοποίησης: Ορισμένες αντιδράσεις χρειάζονται μια ορισμένη ελάχιστη ποσότητα ενέργειας για να ξεκινήσουν. Ένα συμπυκνωμένο διάλυμα παρέχει περισσότερες συγκρούσεις και ως εκ τούτου μεγαλύτερη πιθανότητα να επιτευχθεί αυτή η απαίτηση ενέργειας.
* Ισορροπία μονάδας δίσκου: Ακόμη και αν η αντίδραση είναι αναστρέψιμη, ένα συμπυκνωμένο διάλυμα μπορεί να μετατοπίσει την ισορροπία προς την πλευρά του προϊόντος παρέχοντας υψηλότερη αρχική συγκέντρωση του αντιδραστηρίου.
* Περιορισμοί διαλυτότητας: Μερικές φορές το αντιδραστήριο που πρέπει να εργαστείτε είναι απλά λιγότερο διαλυτό στον διαλύτη. Η χρήση ενός συμπυκνωμένου διαλύματος σάς επιτρέπει να χρησιμοποιείτε υψηλότερη ποσότητα αντιδραστηρίου χωρίς να υπερβείτε το όριο διαλυτότητας.
* Δοκιμές για την εξάρτηση του ρυθμού: Ακόμη και αν δεν υπάρχει παρατηρήσιμη αντίδραση με αραιό διάλυμα, ίσως θελήσετε να δείτε αν ο ρυθμός αντίδρασης αυξάνεται σημαντικά με ένα συμπυκνωμένο διάλυμα. Αυτό μπορεί να σας βοηθήσει να κατανοήσετε τον μηχανισμό αντίδρασης και να προσδιορίσετε το βήμα περιορισμού του ρυθμού.
* Ευαισθησία της ανίχνευσης: Μπορεί να συμβεί μια αντίδραση, αλλά ο σχηματισμός προϊόντος μπορεί να είναι πολύ χαμηλός για να ανιχνευθεί με το αραιό διάλυμα. Η χρήση ενός συμπυκνωμένου διαλύματος μπορεί να αυξήσει την ποσότητα του διαμορφωμένου προϊόντος, καθιστώντας ευκολότερη την ανίχνευση και την ανάλυση.
Σημαντική σημείωση: Είναι σημαντικό να είστε προσεκτικοί όταν εργάζεστε με συγκεντρωμένα διαλύματα, καθώς μπορούν να είναι πιο επικίνδυνα λόγω της υψηλότερης αντιδραστικότητας και του δυναμικού τους για εξωθερμικές αντιδράσεις.
Επιτρέψτε μου να ξέρω αν έχετε μια συγκεκριμένη αντίδραση στο μυαλό. Μπορεί να μπορώ να παράσχω πιο προσαρμοσμένες εξηγήσεις!