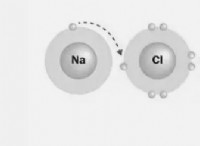
Γιατί τα κατιονικά μοριακά ιόντα είναι μεγαλύτερα από ανιονικά;
1. Πυρηνικό φορτίο: Ένα υψηλότερο πυρηνικό φορτίο (περισσότερα πρωτόνια στον πυρήνα) θα οδηγήσει σε ισχυρότερη έλξη για τα ηλεκτρόνια, τραβώντας τα πιο κοντά και καθιστώντας το ιόν μικρότερο.
2. Αριθμός ηλεκτρονίων: Η απώλεια ηλεκτρόνων (σχηματίζοντας κατιόν) οδηγεί γενικά σε ένα μικρότερο ιόν επειδή υπάρχουν λιγότερες ανταπόκριση ηλεκτρονίων-ηλεκτρονίων. Η απόκτηση ηλεκτρόνων (σχηματίζοντας ένα ανιόν) οδηγεί γενικά σε ένα μεγαλύτερο ιόν λόγω αυξημένων αποκομιδών ηλεκτρονίων-ηλεκτρονίων.
3. Διαμόρφωση ηλεκτρονίων: Η διάταξη των ηλεκτρονίων στα τροχιακά επηρεάζει το μέγεθος. Τα ηλεκτρόνια στα εξωτερικά κελύφη βιώνουν λιγότερη έλξη από τον πυρήνα και συμβάλλουν σε ένα μεγαλύτερο ιόν.
Παράδειγμα:
* νάτριο (Na) έναντι ιόντος νατρίου (Na+): Το ιόν νατρίου είναι μικρότερο από το ουδέτερο άτομο νατρίου, επειδή έχει χάσει ένα ηλεκτρόνιο, μειώνοντας τις αντλίες ηλεκτρονίων-ηλεκτρονίων.
* οξυγόνο (o) έναντι ιόντων οξειδίου (O2-): Το ιόν οξειδίου είναι μεγαλύτερο από το ουδέτερο άτομο οξυγόνου επειδή έχει κερδίσει δύο ηλεκτρόνια, αυξάνοντας τις ανταπόκριση ηλεκτρονίων-ηλεκτρονίων.
Επομένως, δεν είναι δυνατόν να δημιουργηθεί μια γενική δήλωση σχετικά με τα κατιονικά μοριακά ιόντα που είναι πάντα μεγαλύτερα από τα ανιονικά. Το μέγεθος ενός ιόντος εξαρτάται από το συγκεκριμένο στοιχείο και από τον αριθμό των ηλεκτρονίων που έχουν αποκτηθεί ή χαθεί.
Σημαντική σημείωση: Η έννοια του "μεγαλύτερου" μπορεί επίσης να αναφέρεται στο χρέωση του ιόντος. Σε αυτή την περίπτωση, είναι αλήθεια ότι ένα κατιόν έχει θετικό φορτίο, ενώ ένα ανιόν έχει αρνητικό φορτίο. Ωστόσο, αυτό δεν σχετίζεται με το μέγεθος των ιόντων.