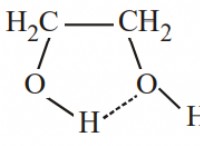
Τι είναι το μόριο υδροξειδίου;
Εδώ είναι μια κατανομή:
* οξυγόνο: Το οξυγόνο είναι ένα εξαιρετικά ηλεκτροαρνητικό στοιχείο, που σημαίνει ότι προσελκύει έντονα ηλεκτρόνια.
* υδρογόνο: Το υδρογόνο είναι σχετικά ηλεκτροθετικό, που σημαίνει ότι έχει πιο αδύναμη συγκράτηση στα ηλεκτρόνια του.
* δεσμός: Τα άτομα οξυγόνου και υδρογόνου μοιράζονται ηλεκτρόνια, σχηματίζοντας ομοιοπολικό δεσμό. Ωστόσο, το άτομο οξυγόνου προσελκύει πιο έντονα τα κοινά ηλεκτρόνια, με αποτέλεσμα ένα μερικό αρνητικό φορτίο στο άτομο οξυγόνου και ένα μερικό θετικό φορτίο στο άτομο υδρογόνου.
* αρνητική χρέωση: Το ιόν υδροξειδίου έχει κερδίσει ένα επιπλέον ηλεκτρόνιο, δίνοντάς του ένα καθαρό αρνητικό φορτίο.
Ιδιότητες κλειδιού:
* Ισχυρή βάση: Τα ιόντα υδροξειδίου είναι εξαιρετικά αντιδραστικά και δρουν ως ισχυρές βάσεις. Δέχονται εύκολα πρωτόνια (h
* Βρέθηκαν σε πολλές ενώσεις: Τα ιόντα υδροξειδίου είναι ένα θεμελιώδες συστατικό πολλών ανόργανων και οργανικών ενώσεων, όπως:
* νερό (h
* αλκαλικά (υδροξείδια): Αυτές είναι ενώσεις που περιέχουν ιόντα υδροξειδίου, όπως υδροξείδιο του νατρίου (ΝΑΟΗ) και υδροξείδιο του καλίου (ΚΟΗ).
* μεταλλικά υδροξείδια: Πολλά μέταλλα σχηματίζουν υδροξείδια, όπως υδροξείδιο του χαλκού (Cu (OH)
Σημασία:
* Χημεία: Τα ιόντα υδροξειδίου διαδραματίζουν κρίσιμο ρόλο στη χημεία βάσης οξέος, επηρεάζοντας το ρΗ και τις χημικές αντιδράσεις.
* Βιολογία: Τα ιόντα υδροξειδίου είναι απαραίτητα για πολλές βιολογικές διεργασίες, συμπεριλαμβανομένης της κυτταρικής αναπνοής και της ρύθμισης του ρΗ στο σώμα.
* Βιομηχανία: Τα ιόντα υδροξειδίου χρησιμοποιούνται σε διάφορες βιομηχανικές διεργασίες, όπως η παραγωγή σαπουνιού, χαρτιού και αλουμινίου.
Σημείωση: Ο όρος "υδροξείδιο" χρησιμοποιείται μερικές φορές για να αναφέρεται τόσο στο ιόν υδροξειδίου (OH